Alessandro José Rodrigues Daré; Leonardo Cunha Castro; Marina Rodrigues de Sunti
DOI: 10.17545/eOftalmo/2022.0005
RESUMO
A degeneração macular relacionada à idade é a principal causa de cegueira irreversível no mundo desenvolvido. Existem algumas opções de tratamento eficazes para degeneração macular relacionada à idade neovascular, sendo a estratégia ‘tratar e estender’ a mais recente e a preferida pelos oftalmologistas, onde as injeções são realizadas mensalmente até que nenhum sinal de atividade da doença, como fluido intrarretiniano ou sub-retiniano, seja evidenciado na OCT, seguido por uma extensão gradual do intervalo de tratamento por 2 semanas. O que ainda não é consagrado é o máximo intervalo eficaz entre as aplicações; neste relato de caso demonstramos uma eficácia em um intervalo maior do que o descrito na literatura, sendo, portanto, necessária futuras investigações para essa determinação.
Palavras-chave: Degeneração da mácula e do polo posterior; Membrana neovascular subretiniana ativa; Neovascularização de coróide; Estratégia tratar e estender.
ABSTRACT
Age-related macular degeneration is the principal cause of irreversible blindness in the developed world. There are some effective treatment options for neovascular age-related macular degeneration, with the current and preferred choice by ophthalmologists known as the ‘treat and extend’ (T&E) strategy. Injections are administered monthly until no sign of the disease activity, such as intraretinal fluid or subretinal, is observed on OCT, followed by a gradual extension of the treatment interval by two weeks. However, the maximum effective interval between injection applications is not yet established. This case report demonstrated the efficacy in a greater range than described in the literature; therefore, further investigations are necessary for the maximum effective interval determination.
Keywords: Mmacula and posterior pole degeneration; Active subretinal neovascular membrane; Choroidal neovascularization; Treat and extend strategy.
INTRODUÇÃO
A degeneração macular relacionada à idade (DMRI) é a principal causa de cegueira irreversível no mundo desenvolvido. A introdução do uso de medicamentos antiangiogênicos intravítreos transformou a forma com a DMRI úmida (ou neovascular) é tratada, possibilitando não só a prevenção da piora da acuidade visual como ocorria nos tratamentos com fototerapia (fotocoagulação da membrana neovascular, terapia fotodinâmica, entre outras), mas prevenindo a perda visual moderada em 90% a 95% dos pacientes e possibilitando a melhora visual de 15 letras ou mais em 33% e 40% dos pacientes, respectivamente nos estudos pivotais MARINA E ANCHOR. Em busca de reduzir o inconveniente de injeções intravítreas mensais, alguns protocolos de tratamento foram desenvolvidos para reduzir a frequência de tratamento e das visitas dos pacientes, sem comprometer os resultados do tratamento mensal. Dentre os protocolos de tratamento desenvolvidos, a estratégia Tratar e Estender (T&E) teve ampla aceitação pelos retinólogos1 por reduzir o número de sessões de tratamento e o número de consultas necessárias do paciente. Em resumo, a estratégia Tratar e Estender consiste em realizar injeções intravítreas mensalmente até que nenhum sinal de atividade da doença seja notado, como fluido intrarretiniano ou sub-retiniano evidenciado na tomografia de coerência óptica (OCT), seguido por uma extensão gradual do intervalo de tratamento por 2 semanas desde que não haja recorrência de atividade da membrana neovascular subretiniana. O que ainda não é consagrado é o intervalo máximo seguro entre as aplicações; a maioria dos estudos citam 12 semanas como intervalo máximo de segurança. Neste caso, demonstramos um paciente com DMRI úmida tratado com injeções intravítreas de medicamento antiangiogênico onde foi possível realizar a estratégia Tratar e Estender até um intervalo maior, de 16 semanas, mantendo a eficácia e segurança do tratamento.
RELATO DE CASO
Paciente feminina, 77 anos, branca, aposentada, relatava baixa da acuidade visual (BAV) em olho esquerdo (OE), há 3 meses. Portadora de hipertensão arterial sistêmica há 10 anos, em tratamento com losartana potássica 50mg/dia, e diabetes mellitus há 10 anos, em tratamento com cloridrato de pioglitazona 30mg/dia e cloridrato de metformina 1000mg/dia. Realizou facoemulsificação com implante de lente intraocular (LIO) em ambos os olhos há 6 anos. Negava trauma ocular.
Apresentava ao exame oftalmológico de entrada acuidade visual para longe (AV P/L) igual a 20/25-1 em olho direito (OD) e 20/80+2 em OE. Ortofórica no teste de cobertura para longe e para perto, sem correção. Sem alterações nas versões. Reflexos pupilares, direto e consensual, preservados. À biomicroscopia anterior apresentava lente intraocular centrada, capsulotomia posterior, sem outras alterações significativas. A pressão intraocular era 13 mmHg em ambos os olhos. À fundoscoscopia em AO (Figuras 1A e 1B): nervo óptico (NO) corado, bem delimitado e com escavação 0,6, vasos de calibre preservados, região macular com hiperpigmentações, drusas de coróide e rarefação de EPR e periferia sem alterações; em OE apresentava membrana epirretiniana (MER) em região macular e hipopigmentação parafoveal temporal com hemorragia intra-retiniana adjacente, sendo os achados ressaltados pelas RED FREE (Figuras 2A e 2B). À autofluorescência (Figuras 3A e 3B) notam-se pontos hipoautofluorescentes intercalados com pontos hiperautofluorescentes em região macular em AO. A OCT (Figuras 4A e 4B) evidenciava pontos elevados hiperrefletivos ao nível do complexo EPR/membrana de Bruch compatíveis com drusas em ambos os olhos. No olho esquerdo evidenciava-se a presença de MER e de material hiperrefletivo sub-retiniano com fluido sub-retiniano adjacente. À angiografia fluorescente (Figura 5 A - F) notavam-se áreas de hiperfluorescência por defeito em janela em região macular em ambos os olhos. No olho esquerdo evidenciou hiperfluorescência tardia por extravasamento de contraste em região macular compatível com membrana neovascular subretiniana do tipo oculta.
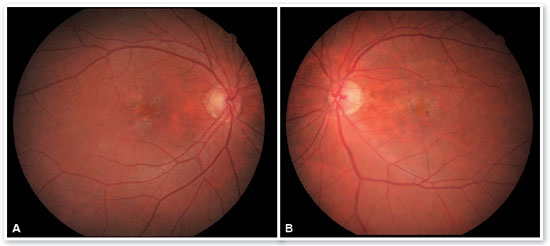
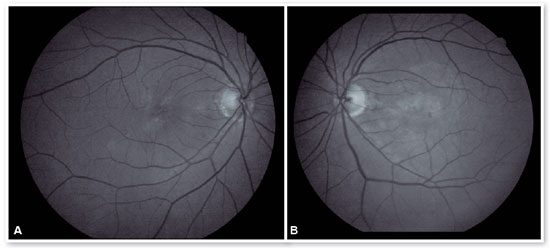
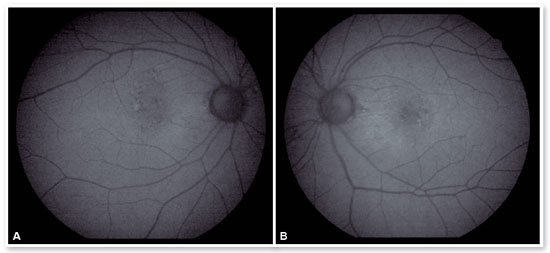
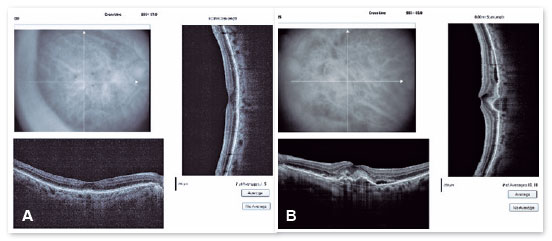
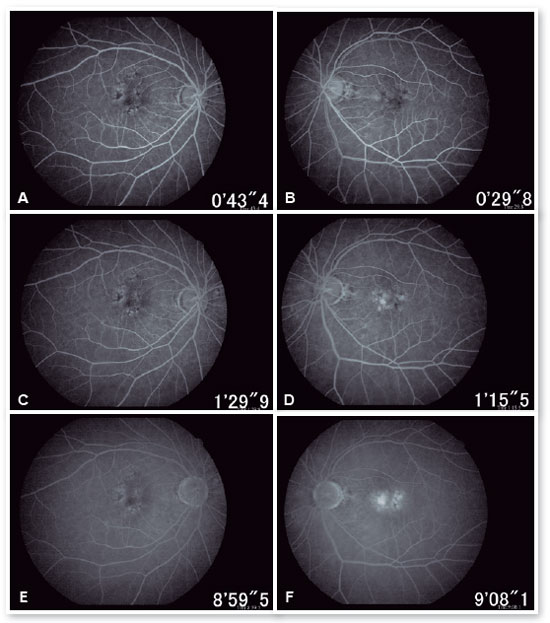
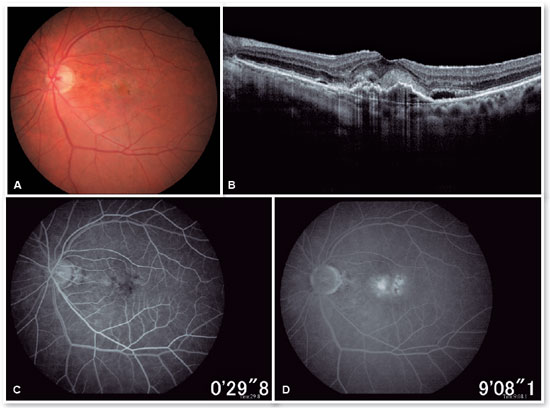
Ao fazer a análise multimodal (Figuras 6 A - D) foi feito o diagnóstico de DMRI seca em OD e exsudativa em OE em atividade, foi iniciado tratamento com injeções intravítreas (IV) de medicamento antiangiogênico (ranibizumabe 10mg/ml) em OE.
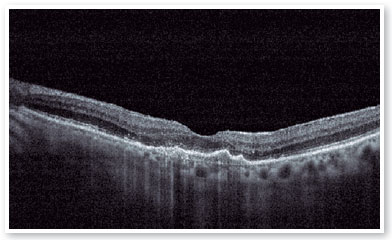
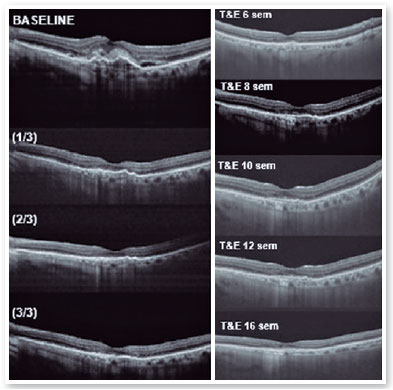
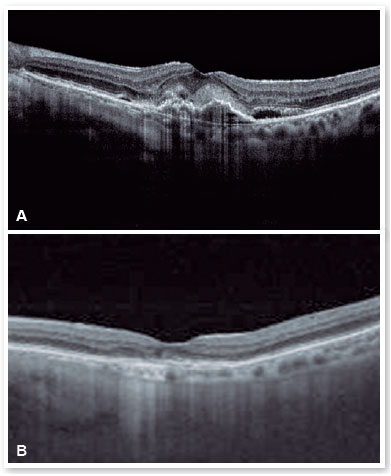
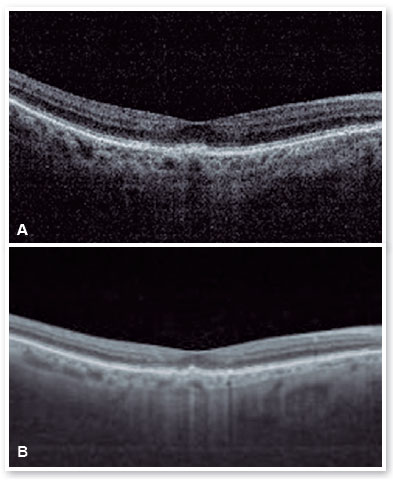
Após a realização da dose de carga com 3 injeções IV mensais, notou-se uma melhora importante do material hiperrefletivo sub-retiniano e resolução completa do fluído sub-retiniano (Figura 7), sendo optado pelo início da estratégia T&E, com incrementos de 2 semanas entre a aplicações até atingir o intervalo de 12 semanas, que foi mantido por duas visitas consecutivas, sem recidiva do fluído; optamos, então, por aumentar o espaçamento para 14 semanas, porém, por motivos pessoais, a paciente retornou com 17 semanas, mantendo sem recidiva do fluído e com melhora importante anatômica e funcional (AV P/L OE: 20/40). Optou-se então por manter o tratamento com manutenção do intervalo de tratamento de 16 semanas, não ocorrendo recidiva de atividade da membrana neovascular subretiniana durante o período de acompanhamento (19 meses). Nas Figuras 8 e 9 podemos fazer o comparativo desde o baseline até atingir o intervalo de 16 semana. O olho direito manteve-se estável durante todo o período de acompanhamento da paciente (Figura 10).
DISCUSSÃO
A DMRI é a principal causa de cegueira irreversível no mundo desenvolvido. Estratégias de aplicação mensal ou conforme a necessidade (PRN) de medicamento antiangiogênico intravítreo foram estabelecidas como opções de tratamento eficazes para DMRI neovascular. Mais recentemente, o regime T&E foi adotado na prática clínica, onde a decisão para cada injeção e o intervalo de tratamento é baseado na resposta do paciente até a última injeção2,3. Ambas as técnicas resultam em ganhos visuais e anatômicos comparáveis, entretanto com um número menor de visitas e injeções intravítreas em favor do regime T&E1,4.
Atualmente, T&E é a estratégia de tratamento preferido pela maioria dos especialistas em retina1, pois representa uma opção econômica e centrada no paciente, fornecendo um tratamento individualizado, reduzindo a carga de tratamento ao estender os intervalos de injeção quando possível1,4.
As injeções são realizadas mensalmente até que nenhum sinal de atividade da doença, como fluido intrarretiniano ou sub-retiniano, seja evidenciado na OCT, seguido por uma extensão gradual do intervalo de tratamento por 2 semanas até um máximo de 12 semanas5. O máximo intervalo entre as injeções ainda não é consagrado; no maior estudo prospectivo de T&E, até o momento da escrita deste artigo, o aumento de intervalo de duas semanas, atingiu um intervalo máximo de 12 semanas5.
A duração da supressão do VEGF-A difere entre pacientes6, portanto o ajuste no intervalo entre as aplicações baseado no resultado anatômico e funcional individual de cada paciente, permite tratar conforme necessidade, atingindo resultado ótimo enquanto reduz a frequência de visitas clínicas para além de 12 semanas. Os resultados do ALTAIR7 indicam que, com regime T&E, intervalo de 12 semanas ou mais podem ser atingidos em aproximadamente 57-60% dos pacientes, sendo que 41-46% atingiram o intervalo máximo de 16 semanas ao final de 2 anos.
No caso apresentado mantivemos o intervalo de 12 semanas, por 2 vezes consecutivas e como o quadro manteve estável sem recidiva do fluido retiniano ou piora da acuidade visual, optamos por aumentar o intervalo para 14 semanas; porém a paciente, por motivos pessoais, compareceu apenas após 17 semanas após a última injeção IV, mantendo a melhora anatômica e funcional (melhora da AV em comparação com a linha de base); por este motivo, mantivemos o espaçamento entre as injeções para 16 semanas, sem recidiva de atividade da Membrana Neovascular Subretiniana durante o período de acompanhamento (19 meses).
Até o momento, a maior parte dos estudos demonstraram eficácia e segurança com intervalo entre as injeções de até 12 semanas, consagrando este como intervalo máximo na prática clínica. Neste caso, foi demonstrado a eficácia com um intervalo maior, de 16 semanas, sendo, portanto, necessário mais estudos sobre a determinação do intervalo máximo eficaz.
REFERÊNCIAS
1. Wykoff CC, Croft DE, Brown DM, Wang R, Payne JF, Clark L, Abdelfattah NS, Sadda SR, TREX-AMD Study Group. Prospective trial of treat-and-extend versus monthly dosing for neovascular age-related macular degeneration. TREX-AMD 1-year results. Ophthalmology. 2015;122(12):2514-22.
2. Spaide RF. Ranibizumab according to need: a treatment for age-related macular degeneration. Am J Ophthalmol. 2007;143(4): 679-80.
3. Oubraham H, Cohen SY, Samimi S, Marotte D, Bouzaher I, Bonicel P, et al. Inject and extend dosing versus dosing as needed: a comparative retrospective study of Ranibizumab in exudative age-related macular degeneration. Retina. 2011;31(1):26-30.
4. Wykoff CC, Ou WC, Brown DM, Croft DE, Wang R, Payne JF, Clark WL, Abdelfattah NS, Sadda SR, TREX-AMD Study Group. Randomized Trial of Treat-and-Extend versus Monthly Dosing for Neovascular Age-Related Macular Degeneration: 2-Year Results of the TREX-AMD Study. Ophthalmol Retina. 2017;1(4):314-21.
5. Mantel I, Niderprim SA, Gianniou C, Deli A, Ambresin A. Reducing the clinical burden of ranibizumab treatment for neovascular age-related macular degeneration using an individually planned regimen. Br J Ophthalmol. 2014;98(9):1192-6.
6. Fauser S, Muether PS. Clinical correlation to differences in ranibizumab and aflibercept vascular endothelial growth factor suppression times. Br J Ophthalmol. 2016;100(11):1494-8.
7. Ohji M, Takahashi K, Okada AA, Kobayashi M, Matsuda Y, Terano Y, ALTAIR Investigators. Efficacy and Safety of Intravitreal Aflibercept Treatand- Extend Regimens in Exudative Age-Related Macular Degeneration: 52- and 96-Week Findings from ALTAIR, A Randomized Controlled Trial. Adv Ther. 2020;37(3):1173-87.
INFORMAÇÃO DOS AUTORES


Financiamento: Declaram não haver
Conflitos de Interesse: Declaram não haver
Recebido em:
24 de Junho de 2021.
Aceito em:
1 de Junho de 2022.