Annelise Lídice Francisquini Fernandes Marra1; Cássio Augusto Macanhão2; Fernando dos Reis Spada3; Astor Grumann Júnior4
DOI: 10.17545/eOftalmo/2021.0022
RESUMO
OBJETIVOS: O objetivo deste estudo foi analisar a associação das diferentes fórmulas para o cálculo da lente intraocular com o resultado refrativo na cirurgia de catarata.
MÉTODOS: Coorte histórica incluindo 200 olhos de 200 pacientes submetidos à facoemulsificação com colocação da lente intraocular (LIO) esférica. Os dados foram tabulados no software Windows Excel e exportados para o programa Statistical Package for the Social Sciences (SPSS). Foi utilizado o teste T de Student e o mesmo nível de significância (p<0,05) em todas as análises.
RESULTADOS: Foram classificados como sucesso cirúrgico os 165 pacientes com refração final de 0,00D (±0,5D), sendo que 140 (83,33%) deles usaram a fórmula SRKT. Foi, ainda, considerado sucesso biométrico aqueles pacientes que obtiveram refração ±0,5D no esférico em relação à refração esperada pela sua biometria, deste modo 49,5% atingiram o sucesso biométrico. Destes: 46.4% tiveram sucesso biométrico com Hoffer Q, 48,8% com SRKT, e 50% com Haigis.
CONCLUSÃO: A fórmula SRKT e Hoffer Q demonstraram uma boa precisão para o sucesso cirúrgico e uma precisão mediana para calcular o sucesso biométrico em olhos de comprimento axial médio. Houve um melhor resultado para o sucesso biométrico nos pacientes míopes no pré-operatório do que nos hipermetropes.
Palavras-chave: Catarata; Biometria; Facoemulsificação; Erros de refração.
ABSTRACT
PURPOSEE: This study has as objective to analyze the association of different formulas on intraocular lenses calculation with the refractive result on cataract surgery
METHODS: Retrospective cohort study including 200 eyes from 200 patients submitted to phacoemulsification with the insertion of the spherical intraocular lens (IOL). The data was arranged on Windows Excel software and exported to the Statistical Package for the Social Sciences (SPSS) program. The Student T test was used with the same level of significance (p<0.05) in all analyses.
RESULTS: The 165 patients classified as surgical success were the ones with final refraction of 0.00D (±0.5D), of whom 140 (83.33%) used the formula SRKT. It was yet considered biometric success those patients who obtained ±0.5D refraction on the spherical in relation to the expected refraction by its biometry, this way 49.5% reached biometric success. From these: 46.4% achieved biometric success with Hoffer Q, 48.8% with SRKT, and 50% with Haigis.
CONCLUSION: The SRKT and Hoffer Q formulas have showed good precision for surgical success and regular precision to evaluate biometric success on eyes with average axial length. There was a better result on the biometric success of myopic patients on the preoperative than the hyper myopic ones.
Keywords: Cataract; Biometry; Phacoemulsification; Refractive Errors.
INTRODUÇÃO
A visão humana decorre do funcionamento integrado dos subsistemas retina, pupila, córnea, íris, nervo óptico e cristalino. A formação de imagens é obtida a partir da focalização da luz na retina por meio do cristalino, que gera imagens através do nervo óptico1. Para que ocorra transmissão de luz com clareza, é necessário que haja transparência do cristalino, a qual depende de células com formato correto e do arranjo compacto de suas proteínas2. Assim, a catarata pode ser definida como opacidade do cristalino3. Em decorrência disto, a imagem perderá sua nitidez e a acuidade visual será reduzida4.
A estatística mundial relata que o principal fator de risco para a formação de catarata é o envelhecimento5. Além deste, há outras causas possíveis tais como: trauma ocular, tabagismo, radiação ultravioleta, diabetes e a catarata congênita6.
Atualmente, a facoemulsificação é a técnica cirúrgica mais utilizada na maioria dos países desenvolvidos, devido à possibilidade de rápida recuperação visual e ao reduzido índice de complicações pré e pós-operatórias7. Esta técnica é realizada por meio de uma pequena incisão na córnea através da qual se fragmenta e aspira o cristalino opacificado8, substituindo-o por uma lente intraocular (LIO) artificial9.
Observa-se que os pacientes que serão submetidos à facoemulsificação possuem expectativa de melhor visão, bem como, minimização do erro refrativo pós-operatório, que poderá resultar na eliminação da necessidade do auxílio dos óculos10. Para isto é fundamental o cálculo preciso e o adequado implante da LIO11.
Visando obter maior êxito do procedimento de implantação da LIO, é fundamental que se realizem as medidas do comprimento axial, da ceratometria e da profundidade da câmara anterior12. Isso, pode ser obtido pelo biômetro ultrassônico, o qual emite sons e geram ecos refletidos sendo propagados entre as estruturas do globo ocular13.
Ainda, nesse sentido, existe um aparelho denominado biômetro óptico que, não possui contato com o paciente, dispõe de um feixe de luz para obter as medidas necessárias para o cálculo do comprimento axial. De maneira similar à da tomografia de coerência óptica, ele utiliza a técnica de interferometria de coerência parcial (ICP)13.
Segundo de Monteiro et al.13, pelo método da ICP, o comprimento axial é determinado por dois feixes de luz coaxiais que incidem sobre a superfície anterior da córnea e sobre o epitélio pigmentado da retina, eliminando a influência dos movimentos longitudinais do olho. É importante ressaltar que, estudos norte-americanos e europeus afirmaram que 95% dos casos de catarata podem ser examinados através da biometria óptica13.
Pode-se perceber que a precisão biométrica, associada à técnica cirúrgica aprimorada e à evolução das LIOs, podem corrigir ametropias pré-existentes, além de corrigir a catarata do paciente. Portanto, a biometria óptica é o principal exame oftalmológico para calcular a LIO e é um método capaz de estimar com precisão o grau esférico final do paciente, tornando assim a facectomia um procedimento com elevada taxa de sucesso e baixo índice de complicação12.
Surge assim, a necessidade de calcular com exatidão o poder dióptrico da LIO14. São conhecidas várias fórmulas para determinar a escolha ideal da lente a ser implantada. As fórmulas de primeira geração e as de segunda geração (SRK e SRK II) apresentaram melhores resultados em olhos com comprimento axial médio (22 a 24,50mm). Já com as fórmulas de terceira geração (SRK T e Hoffer-Q, Holladay) obteve-se significantes melhorias nos resultados em olhos de comprimento axial maior que 24,50mm e menor que 22mm respectivamente15. As fórmulas de quarta geração (Holladay 2 e Haigis) indicam ter solucionado problemas decorrentes de diferentes dimensões do globo ocular, com exceção na miopia extrema16,17. E, finalmente, as fórmulas de quinta geração, Olsen e Barrett Universal II. Esta última denominada universal porque possui bom desempenho no cálculo de olhos com os todos os comprimentos axiais18. Estas gerações de cálculo da LIO fundamentam-se na medida profundidade da câmara anterior (PCA), do comprimento axial (AL), da espessura do cristalino (LT) e da ceratometria (K)13.
Como já comentado, o cálculo da LIO na cirurgia de catarata ainda é um desafio. Portanto para que se tenha resultados refrativos pós-operatórios com significativo sucesso, torna-se essencial que sejam validadas e avaliadas novas fórmulas que propiciem a potência de cálculo de LIOs19. Nesse sentido, o presente estudo tem como objetivo analisar as diferentes fórmulas para o cálculo da lente intraocular e o resultado refrativo na cirurgia de catarata.
MÉTODOS
No presente estudo, do tipo coorte histórica, foram avaliados 200 olhos de 200 pacientes que realizaram facoemulsificação com colocação de LIO asférica (modelo SN60WF) no período de janeiro de 2012 a dezembro de 2016.
A acuidade visual pré e pós-operatória foram avaliadas com a melhor correção visual, por meio da escala de Snellen e para fins de análise estatísticos transformadas para a escala de logMAR. A avaliação dos resultados refracionais pós-operatórios foram realizados no mínimo 3 meses após a facoemulsificação.
Foram incluídos pacientes de ambos os sexos, com idade igual ou superior a 18 anos, com diagnóstico de catarata, submetidos à facoemulsificação com implante de LIO asférica, sendo excluídos pacientes que realizaram cirurgia refrativa prévia e pacientes que haviam realizado cirurgia de facoemulsificação no olho contralateral no período de avaliação deste estudo, portanto, foi considerado apenas um olho daqueles pacientes que realizaram esta técnica bilateralmente. A amostra foi selecionada de maneira sequencial e não aleatória no período do estudo.
Para o cálculo da LIO foi utilizado o comprimento axial (AXL), os valores de ceratometria central (K1 e K2), o poder dióptrico esperado da lente intraocular, medidos com a interferometria de coerência parcial sem contato (IOL Master, versão 3.01, Carl Zeiss Meditec, Jena, Alemanha). As LIOs foram calculadas conforme os diferentes comprimentos axiais, utilizando as fórmulas Hoffer Q, SRKT e Haigis. Para fins de análise comparativa, foram utilizadas além das fórmulas já descritas a fórmula de Holladay 1. Comparando, então, os valores obtidos em cada fórmula com o resultado refrativo na cirurgia de catarata. A variável dependente utilizada foi a fórmula utilizada para o cálculo da lente intraocular (Holladay 1, Hoffer Q, SRK/T, Haigis). As variáveis independentes foram as características demográficas: sexo, idade, olho e características clínicas: história de cirurgia oftálmica prévia, comprimento axial ocular (16 a 32 mm) e refração inicial e final (0 a ±10 dioptrias).
Todas as facoemulsificações deste estudo foram realizadas com uma micro-incisão na córnea para a retirada do cristalino opacificado e, posteriormente, para a inserção da LIO. Foi utilizado o facoemulsificador Centurion® da Alcon.
Para fim de análise, no presente estudo, foram considerados o sucesso cirúrgico e o sucesso biométrico. Foram classificados em sucesso cirúrgico, aqueles que após a cirurgia de catarata, atingiram, na avaliação pós-operatória final, uma refração plana ou com variação de ±0,50D no esférico. Já o sucesso biométrico foi definido, a partir da refração esférica esperada, na biometria realizada pelo IOL Master, e comparado com a refração final do paciente. Foram classificados como sucesso biométrico, aqueles pacientes que tiveram, no máximo, uma variação ±0,50D da refração esperada pelo cálculo biométrico.
Os dados qualitativos foram descritos na forma de frequências (simples e relativa) e foram analisados pelo teste do χ quadrado. Os dados quantitativos foram demonstrados pelas medidas de tendência central (média) e suas respectivas medidas de variabilidade/dispersão (Amplitude [máximo e mínimo] e desvio padrão). O valor médio calculado pelas fórmulas foi apresentado para cada grupo das variáveis independentes e a significância das diferenças nas médias calculadas pelo teste T de Student e análise de variância. O nível de significância pré-estabelecido foi de 95% de confiança (p≤0,05).
A coleta de dados foi realizada de acordo com os critérios de inclusão e após aprovação pelo Comitê de Ética em Pesquisa da Universidade do Sul de Santa Catarina (CEP-UNISUL). Aprovado sob o CAAE 80422817.0.0000.5369. As informações foram acessadas por meio de prontuários eletrônicos após a disponibilização da senha pelo guardião dos prontuários.
RESULTADOS
Foram analisados 200 prontuários de pacientes que realizaram cirurgia de facoemulsificação com implante de lente intraocular no período de 2012 a 2016. No que tange as características da amostra, a média de idade dos pacientes submetidos à cirurgia foi de 71,7 (±8,07 DP) anos (35-90 anos) sendo 106 (53%) olhos direitos e 94 (47%) olhos esquerdos. Em relação ao sexo dos pacientes, 128 (64%) eram mulheres e 72 (36%) eram homens.
A acuidade visual pré e pós-operatória avaliada com a melhor correção na escala logMAR, variou de 0,00 a 1,3 (média 0,29, ± 0,23 DP) no pré-operatório e no pós-operatório de 0,00 a 1,00 (média 0,05, ± 0,05 DP). A refração esférica pré-operatória variou de -5,00 a +5,75, com média de +1,27D (±1,82DP) e no pós-operatório de -2,50 a +1,50, tendo uma média final de -0,45D no pós-operatório (±0,48 DP), conforme monstra a tabela 1.
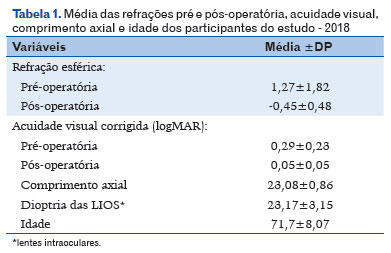
Demonstra-se na mesma tabela, que o comprimento axial variou de 21,14mm a 25,38mm, com média de 23,08mm (±0,86 DP). Entre a dioptrias das lentes intraoculares utilizadas nas cirurgias à média foi de 23,17D (±3,15 DP), variando de 16,50D a 35,00D.
Foram utilizadas as fórmulas SRKT, Hoffer Q e Haigis para cálculo biométrico da LIO no pré-operatório. A fórmula SRKT foi utilizada em 168 (84%) dos pacientes, a Hoffer Q em 28 (14%) e a Haigis em quatro (2%) pacientes.
Transpondo os valores reais dos cálculos biométricos dos 200 pacientes, obtidos no pré-operatório para as demais fórmulas, os valores médios das LIOs foram: com o uso da fórmula SRKT de 23,07D (±3,01 DP), na Hoffer Q de 23,32D (±3,52 DP), na Haigis de 23,25D (±3,47 DP) e na Holladay de 23,07D (±3,47 DP), havendo significância estatística entre as fórmulas e a média das dioptrias das LIOs (p<0,01), exceto entre SRKT e Holladay (p=0,93), como mostra a tabela 2.
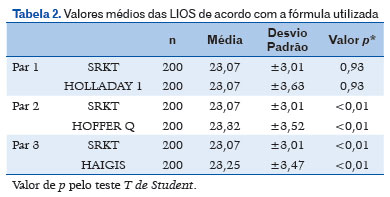
O sucesso cirúrgico, isto é, que obtiveram na avaliação pós-operatória final, uma refração plana ou com variação de ±0,50D no esférico, foi encontrado em 165 (82,5%) dos pacientes e 35 (17,5%) não o obtiveram.
Levando em consideração o sexo e o sucesso cirúrgico, das 128 mulheres da amostra, 106 (82,6%) obtiveram sucesso cirúrgico e dos 72 homens do estudo, 59 (81,9%) o atingiram, não havendo significância estatística no que se refere o sexo e o sucesso cirúrgico (p=0,877).
Dos 165 pacientes que obtiveram sucesso cirúrgico foi atingido 91 (55,2%) em olhos direitos e 74 (44,8%) em olhos esquerdos, não havendo significância estatística entre o olho operado e o sucesso cirúrgico (p=0,186).
No que tange o uso das fórmulas e o sucesso cirúrgico, 168 pacientes em que foi utilizada a fórmula SRKT, obteve-se êxito em 140 (83,3%) pacientes. A média das LIOs foi de 22,84D (±2,88 DP). Caso fosse utilizado nestes 168 pacientes a fórmula Hoffer Q, a média das LIOs seria de 23,09D (±3,35 DP), na Haigis 23,05D (±3,32 DP) e na Holladay 22,98D (±3,1 DP), sendo estatisticamente significativa a diferença das médias das LIOs entre cada fórmula (p<0,01).
Foi considerado sucesso biométrico aqueles pacientes que obtiveram refração mais ou menos 0,5D no esférico em relação à refração esperada pela sua biometria, deste modo 99 (49,5%) atingiram o sucesso biométrico e 101 (50,5%) não o obtiveram, valores demonstrados na Tabela 3.
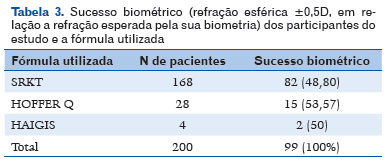
Levando em consideração as 128 mulheres estudadas e o sucesso biométrico, 65 (50,8%) tiveram sucesso biométrico e 63 (48,2%) não tiveram o alcançaram. Já entre os 72 homens, 34 (47,22%) atingiram o sucesso biométrico e 38 (52,8%) não o atingiram, não havendo significância estatística a relação entre os sexos e o sucesso biométrico (p=0,629).
Os olhos direitos operados tiveram um sucesso biométrico em 54 (50,94%) pacientes e nos olhos esquerdos em 45 (47,87%) pacientes, não havendo valor estatístico significativo entre o olho operado e o sucesso do cálculo biométrico (p=0,665).
A ceratometria média nos pacientes em que se atingiu o sucesso biométrico foi de K1 43,48 (±1,82 DP) e K2 44,49 (±1,71DP) e nos que não atingiram sucesso biométrico foi de K1 43,44 (±1,78 DP) e K2 44,28 (±1,82 DP), não havendo significância estatística entre a relação do valor da ceratometria (K1 e K2) e o sucesso biométrico (p=0,175).
Nos 166 pacientes que eram hipermetropes no pré-operatório, a média da refração esférica pós-operatória foi de -0,07D (±0,23 DP) atingindo sucesso biométrico em 77 (46,38%) dos pacientes. Já nos 34 pacientes que eram míopes no pré-operatório, a média da refração esférica pós-operatória foi de -0,26D (±0,19 DP) com sucesso biométrico em 21 pacientes (61,7%).
Os 99 pacientes com sucesso biométrico tiveram uma refração esférica final de -0,18D e os 101 pacientes que não obtiveram sucesso biométrico tiveram uma refração esférica de -0,71D, havendo uma diferença média de refração entre a presença de sucesso e insucesso de -0,53D não sendo estatisticamente significativo (p=0,267).
No que tange o uso das fórmulas e o sucesso biométrico tem-se os seguintes resultados: dos 168 pacientes em que foi utilizada a fórmula SRKT, obteve-se êxito em 82 (48,80%) no sucesso biométrico e 86 (51,20%) não o obtiveram, conforme demonstrado na Tabela 3.
A média da dioptria da lente intraocular calculada pela SRKT e que obteve sucesso biométrico foi de 22,92D (±2,86 DP), caso esses cálculos fossem realizados pela Hoffer Q teríamos uma dioptria média de 23,18 (±3,33 DP), na Haigis de 23,14 (±3,33 DP), e na Holladay 23,07 (±3,10 DP), sendo estatisticamente significativa a diferença das médias das LIOs entre cada fórmula (p<0,01).
Já na fórmula Hoffer Q, utilizada em 28 pacientes, atingiram o sucesso biométrico 15 pacientes (53,57%) e 13 pacientes (46,43%) não, conforme demonstrado na Tabela 3. O valor médio dos 28 pacientes que utilizaram a fórmula Hoffer Q foi de 24,50D (±4,19 DP), caso fosse utilizada a fórmula SRKT teríamos uma LIO média de 24,28D (±3,52), na Haigis de 24,21D (±3,52 DP) e na Holladay de 24,33D (±3,83), sendo estatisticamente significativa a diferença das médias das LIOs entre cada fórmula (p<0,01).
Já o valor médio da LIO, nos pacientes em que tiveram sucesso biométrico com a fórmula Hoffer Q (15 pacientes), foi de 24,13D (±3,52 DP), caso fosse utilizada a fórmula SRKT, a LIO média seria de 23,93D (±4,30 DP), na Haigis seria de 23,93D (±5,10 DP) e na Holladay 24,06 (4,73 DP), sendo estatisticamente significativa a diferença das médias das LIOs entre cada fórmula (p<0,01).
A fórmula de Haigis foi utilizada em 2% da amostra (quatro pacientes), metade deles (dois pacientes) atingiram o sucesso biométrico, conforme demonstrado na tabela 3.
DISCUSSÃO
No atual estudo, não se observou relação entre sucesso cirúrgico e sucesso biométrico com fatores sociodemográficos, como a idade e o sexo dos pacientes. Conforme demonstrado nos estudos de Hayashiet et al.20 e Reitblat et al.21, os quais também não evidenciaram correlação estatística entre essa relação.
Neste estudo, foi comprovado uma melhora substancial na acuidade visual final do paciente após o procedimento cirúrgico, resultando em refração final plana ± 0.5D no esférico (considerado como sucesso cirúrgico) e com acuidade visual média pós-operatória na escala logMAR de 0.05 (±0.05 DP) fato que, também, foi demonstrado na literatura de Chiacchio et al.22, com média da acuidade visual no pré-operatório de 0,64 logMAR e no pós-operatório de 0,09 logMAR.
Na pesquisa coordenada por Aristodemou et al.23, concluiu-se que entre o intervalo de 21,5 a 26 mm no AXL não houve diferença estatisticamente significativa entre as fórmulas utilizadas para o cálculo biométrico, estando em consonância com o atual estudo que utilizou as fórmulas: SRKT, Hoffer Q e Haigis nos pacientes neste intervalo de comprimentos axiais. É importante destacar que, conforme o estudo realizado por Shajari et al.24, no qual houve a avaliação de 9 fórmulas para o cálculo da LIO, concluiu que se obteve maior precisão com a utilização das fórmulas Barrett e Olsen principalmente, sendo fórmulas de 5ª geração. Nesse sentido, em concordância com o presente estudo, determina-se que o uso de diferentes fórmulas (SRKT, Haigis ou Hoffer Q), resulta em valores distintos nas LIOs.
Avaliando o sucesso biométrico, neste estudo 49,5% dos pacientes o atingiram, deste modo pode-se afirmar que aproximadamente metade dos pacientes estudados tiveram uma refração ±0,5D em relação à refração estimada pelo cálculo biométrico. Ao comparar com a literatura, de acordo com Rodrigues et al.12, observou-se que 55% dos indivíduos alcançaram resultados de ± 0,5D.
Já no estudo de Monteiro et al.13, 40,7% dos casos apresentaram refração residual de até ±0,50D utilizando a fórmula SRKT. Sendo que este valor é próximo do encontrado no presente estudo, que obteve 48,8% de sucesso biométrico (refração residual ±0,5D) com o uso da fórmula SRKT. Lagrasta et al.25 em um estudo prospectivo de 33 olhos submetidos a facoemulsificação com implante de lente intraocular utilizando a fórmula de SRKT com comprimento axial de 22,5 a 24,5mm encontrou um erro refracional de ±0,50D em 55% dos pacientes, apresentando comprimento axial e sucesso biométrico semelhantes ao presente estudo.
No estudo de Corrêa et al.14, foram analisados 81 pacientes submetidos a cirurgia de facoemulsificação e implante de lente intraocular, utilizando a fórmula SRKT, com dados epidemiológicos semelhantes, como a média de idade 62,5 anos e, ainda, foi atingido sucesso biométrico com refração residual de ±0,5D em 40,7% dos pacientes, número próximo do sucesso biométrico encontrado no presente estudo.
Ainda no estudo de Rodrigues et al.12, obteve-se sucesso biométrico de ±0,50D de 55% nos olhos direitos e 46% nos olhos esquerdos quando utilizado a fórmula Haigis, porcentagem esta próxima à do estudo atual quando utilizado a fórmula citada. Como a amostra de pacientes em que foi utilizada a fórmula de Haigis foi pequena no presente estudo, não foi possível comparar com exatidão com os dados da literatura. Já Camps et al.26 utilizou a fórmula de Haigis para cálculo em pacientes que foram submetidos a ceratotomia refrativa no passado, atingindo um equivalente esférico plano em 40% dos pacientes e até ±1 em 80% dos pacientes estudados.
Uma das explicações para a diferença entre o sucesso cirúrgico e sucesso biométrico é a experiência do cirurgião ao estimar que as fórmulas de 3ª geração utilizadas possuam uma tendência a hipermetropia. Deste modo, opta-se por utilizar LIOs buscando uma refração final discretamente direcionada a miopia a fim de alcançar a emetropia. Observa-se o anteriormente descrito comparando a refração esférica pré-operatória com média de +1,27D (±1,82 DP) e no pós-operatório de -0,45D (±0,48 DP). É relevante destacar que, neste estudo, observou-se uma diferença refracional média de aproximadamente 0,5D dentre os pacientes que atingiram o sucesso biométrico e os que não o atingiram.
Conforme Rodrigues e cols.12, na seleção da fórmula para pacientes míopes, a fórmula Haigis ou a fórmula SRKT aumentaram a precisão no resultado refrativo e indicam ser fórmulas mais precisas do que a fórmula de Holladay 1. No estudo de Cetinkaya et al.27 em que os pacientes eram alto míopes (AXL 26-33mm), foi utilizada a fórmula de SRKT com refração pós-operatória de ±1D em 51,2% dos pacientes estudados. Ainda, segundo essa literatura, a facoemulsificação permitiu que, em 51,6% dos pacientes com catarata e miopia alta, atingissem a refração pós-operatória dentro do alvo esperado, diferente do presente estudo, em que foi encontrado sucesso biométrico em 61,7% dos pacientes míopes.
Em relação aos pacientes hipermetropes, no estudo de Akaishi et al.28, resultados demostraram melhora estatisticamente significativa na média da acuidade visual pós-operatória em pacientes hipermetropes. Já no presente estudo, os hipermetropes, atingiram uma refração esférica média de -0,07D (±0,23 DP) no pós-operatório. Destes, apenas 77 pacientes (46,38%) atingiram o sucesso biométrico. Assim, pode-se afirmar que os pacientes míopes no pré-operatório tiveram uma tendência superior a atingir o sucesso biométrico do que os pacientes hipermetropes no pré-operatório.
Neste estudo, observou-se que na maioria dos pacientes foram utilizadas fórmulas de 3ª geração (SRKT e Hoffer Q) e em apenas 2% dos pacientes foi utilizada uma fórmula de 4ª geração (Haigis). Apesar dos resultados obtidos demonstrarem semelhança com os resultados registrados na literatura, ou seja, resultado refracional final de plano ±0,5D próximo dos 50%, persiste a incerteza quanto ao uso adequado de uma determinada fórmula e o sucesso cirúrgico e biométrico final. Diante do exposto, na busca do aprimoramento do desempenho das fórmulas para o cálculo da biometria, recomenda-se que sejam consideradas e analisadas as características oculares de cada paciente.
A fórmula SRKT e Hoffer Q demonstraram uma boa precisão para o sucesso cirúrgico e uma precisão mediana para calcular o sucesso biométrico em olhos de comprimento axial médio com o uso do IOL Master, versão 3.01. A fórmula de 4ª geração Haigis não teve uma amostra quantitativa considerável neste trabalho. Houve um melhor resultado para o sucesso biométrico nos pacientes míopes no pré-operatório do que nos hipermetropes. Ressalta-se, ainda, que a experiência do cirurgião foi de extrema importância para o sucesso cirúrgico final dos pacientes. Deste modo, conclui-se que a escolha da fórmula para o cálculo biométrico continua sendo uma decisão desafiadora, devendo-se levar em conta inúmeras variáveis e individualizando cada paciente para obter-se os melhores resultados.
REFERÊNCIAS
1. Acharya RU, Yu W, Zhu K, Nayak J, Lim T-C, Chan JY. Identification of Cataract and Post-cataract Surgery Optical Images Using Artificial Intelligence Techniques. J Med Syst. 2010;34(4):619-28.
2. Figueirêdo SE. Estudo de alterações estruturais nos genes CRYAA, CRYGC E CRYGD em pacientes com catarata congênita de uma população brasileira [tese de doutorado]. Campinas: Universidade Estadual de Campinas; 2013.
3. Sheeladevi S, Lawrenson JG, Fielder AR, Suttle CM. Global prevalence of childhood cataract: a systematic review. Eye. 2016;30(9):1160-9.
4. Grałek M, Kanigowska K, Seroczyńska M. Cataract in children-not only an ophthalmological problem. Medycyna Wieku Rozwojowego. 2007;11(2):227-30.
5. Taleb A, Ávila M, Moreira H. As condições de saúde ocular no Brasil - 2009. 1ed. São Paulo: Conselho Brasileiro de Oftalmologia; 2009.
6. Yi J, Yun J, Li Z-K, Xu C-T, Pan B-R. Epidemiology and molecular genetics of congenital cataracts. Int J Ophthalmol. 2011;4(4):422-32.
7. Nieves-Moreno M, Asorey-García A, Santos-Bueso E, García-Sánchez J. Historia de la cirugía de cataratas (I): desde el abatimiento hasta la extracción. Arch Soc Esp Oftalmol. 2015;e1-3.
8. Desai P, Reidy A, Minassian DC. Profile of patients presenting for cataract surgery in the UK: national data collection. Br J Ophthalmol. 1999;83(8):893-6.
9. Grumann Junior A, Flügel N, Ritta P. An analysis of the visual results when using toric lenses in cataract surgery. Rev Bras Oftalmol. 2015;74(1):12-5.
10. Rubenstein JB, Raciti M. Approaches to corneal astigmatism in cataract surgery. Curr Opin Ophthalmol. 2013;24(1):30-4.
11. Rezende F, Bisol RR, Bisol T. Troca do cristalino com finalidade refrativa (TCR). Rev Bras Oftalmol. 2009;68(3):180-7.
12. Rodrigues WF, Vidal CLL, Mendonça RLA, Silva ER. Biometria ocular, estimativa matemática e variação esférica pós-facectomia. Rev Bras Oftalmol. 2015;74(6):350-4.
13. Monteiro EL, Allemann N. Biometria óptica. Arq Bras Oftalmol. 2001;64(4):367-70.
14. Corrêa ZM da S, Kronbauer FL, Goldhardt R, Marcon ÍM, Bakowicz F. Precisão ecobiométrica da fórmula SRK/T na facoemulsificação. Arq Bras Oftalmol. 2001;64(3):233-7.
15. Retzlaff JA, Sanders DR, Kraff MC. Development of the SRK/T intraocular lens implant power calculation formula. J Cataract Refract Surg. 1990;16(3):333-40.
16. Zaldivar R, Shultz MC, Davidorf JM, Holladay JT. Intraocular lens power calculations in patients with extreme myopia. J Cataract Refract Surg. 2000;26(5):668-74.
17. Hoffer KJ. Clinical results using the Holladay 2 intraocular lens power formula. J Cataract Refract Surg. 2000;26(8):1233-7.
18. Melles RB, Holladay JT, Chang WJ. Accuracy of Intraocular Lens Calculation Formulas. Am Acad Ophthalmol. 2018;125(2):169-78.
19. Feijóo B, Ferreira T, Zabala L, Guerra P, Gonçalves C, Couceiro J, et al. Comparação de metodologias actuais para cálclo da potência da lente intra-ocular. Revista Sociedade Portuguesa de Oftalmologia. 2017;41(4):9-16.
20. Hayashi K, Ogawa S, Yoshida M, Yoshimura K. Influence of Patient Age on Intraocular Lens Power Prediction Error. Am J Ophthalmol. 2016;(170):232-37.
21. Reitblat O, Levy A, Kleinmann G, Abulafia A, Assia EI. Effect of posterior corneal astigmatism on power calculation and alignment of toric intraocular lenses: Comparison of methodologies. J Cataract Refract Surg. 2016; 42(2):217-25.
22. Chiacchio BB, Sato RM, Siqueira RB, Marques FF. Fidelidade do “potential acuity meter” (PAM) no prognóstico da acuidade visual pós-operatória de cirurgia de catarata. Arq Bras Oftalmol. 2008;71(6):805-8.
23. Aristodemou P, Knox Cartwright NE, Sparrow JM, Johnston RL. Formula choice: Hoffer Q, Holladay 1, or SRK/T and refractive outcomes in 8108 eyes after cataract surgery with biometry by partial coherence interferometry. J Cataract Refract Surg. 2011; 37(1):63-71.
24. Shajari M, Kolb CM, Petermann K, Böhm M, Herzog M, de’Lorenzo N, et al. Comparison of 9 modern intraocular lens power calculation formulas for a quadrifocal intraocular lens. J Cataract Refract Surg. 2018;44(8):942-48.
25. Lagrasta JM. Clinical results in phacoemulsification using the SRK/T formula. Arq Bras Oftalmol. 2009;72(2):189-93.
26. Camps VJ, Lorens DPP, Fez D, Coloma P, Caballero MT, Garcia C, et al. Algorithm for Correcting the Keratometric Estimation Error in Normal Eyes. Optom Vis Sci. 2012;89(2):221-8.
27. Cetinkaya S, Acir NO, Cetinkaya YF, Dadaci Z, Yener HI, Saglam F. Phacoemulsification in eyes with cataract and high myopia. Arq Bras Oftalmol. 2015;78(5):286-9.
28. Akaishi L, Tzelikis PF. Primary piggyback implantation using the ReSTOR intraocular lens: case series. J Cataract Refract Surg. 2007;33(5):791-5
INFORMAÇÃO DOS AUTORES



Financiamento: Declaram não haver
Conflitos de Interesse: Declaram não haver
Recebido em:
16 de Junho de 2020.
Aceito em:
28 de Janeiro de 2021.