Daniel Amorim Leite1; Daniel Vítor Vasconcelos Santos2; Fábio Medina Rodrigues Rocha3; Marco Antônio Guarino Tanure4
DOI: 10.17545/e-oftalmo.cbo/2015.36
RESUMO
OBJETIVO: O objetivo deste estudo foi apresentar uma visão abrangente dos transplantes endoteliais, explicando as técnicas realizadas atualmente, vantagens, desvantagens e os principais desafios de sua evolução.
MÉTODOS: Estudo descritivo das principais técnicas de transplante endotelial realizadas, com base nos principais artigos publicados sobre o tema.
RESULTADOS: Existe uma considerável evolução dos transplantes endoteliais nas últimas décadas. Dessa forma, o número de transplantes realizados apresenta um crescente. Apesar dos avanços e vantagens dos endoteliais, a avaliação da qualidade visual dos enxertos preparados ainda é um desafio.
CONCLUSÃO: A análise da interface óptica dos transplantes endoteliais é um dos caminhos para o entendimento da variação da qualidade visual de pacientes submetidos a diferentes técnicas de preparo dos enxertos corneanos. Esta análise poderá ajudar a compreender resultados visuais insatisfatórios com os transplantes endoteliais, apesar do excelente resultado anatômico.
Palavras-chave: Transplante de Córnea, Ceratoplastia Endotelial com Remoção da Lâmina, Limitante Posterior, Epitélio posterior
ABSTRACT
OBJECTIVE: This study aimed to present a broad overview of endothelial transplants and outline the techniques currently used and the advantages, disadvantages, and main challenges of advancements in the procedure.
METHODS: A descriptive study on the most frequently used techniques for endothelial transplantation based on the main articles published on the topic.
RESULTS: There have been considerable advancements in endothelial transplants in recent decades. Thus, the number of transplants performed has increased. Despite these advances and the advantages of endothelial transplantation, the assessment of the visual quality of the grafts is yet a challenge.
RESULTS: Analysis of the optical interface of endothelial transplants can be used to understand variations in visual quality experienced by patients who underwent different corneal graft preparation techniques. This analysis may aid in the understanding of unsatisfactory visual results after endothelial transplants, which may occur despite excellent anatomical results.
Keywords: Corneal Transplantation, Descemet Stripping, Endothelial Keratoplasty Endothelium, Corneal
INTRODUÇÃO
A córnea é composta por cinco camadas: epitélio, camada de Bowman, estroma, membrana de Descemet e endotélio.1 Em 2013 foi proposto por Dua a presença de uma camada pré-Descemet, que recebeu o seu nome. Tal observação foi decorrente de estudo em córneas submetidas a transplante lamelar anterior através da técnica de big-bubble.2
O endotélio funciona como uma bomba permitindo a deturgescência e a consequente transparência da córnea. A perda endotelial pode ocorrer devido à idade avançada, doenças hereditárias ou trauma cirúrgico, resultando em disfunção endotelial com subsequente edema da córnea.3 O endotélio humano não tem a capacidade de replicar-se in vivo, possuindo o adulto jovem uma contagem de 3500 células por milímetro quadrado e uma espessura corneana central média de 550 micrômetros.4
A distrofia endotelial de Fuchs foi a principal causa de transplante penetrante nos EUA em 2011 (20,8%), sendo também a indicação mais comum para transplante endotelial (48%).5 A ceratopatia bolhosa pseudofácica constitui outra indicação para a realização de transplante endotelial. Em 2000, nos EUA, 22,3% dos transplantes foram realizados por esse motivo. Entretanto, esse número foi reduzido com a melhoria das técnicas de facoemulsificação.6 Constitui ainda a segunda causa de indicação de transplantes endoteliais nos EUA, sendo responsável por 19,2%.5 O desencadeamento de um quadro de ceratopatia bolhosa associa-se com a presença muitas vezes subclínica da distrofia endotelial de Fuchs. O quadro pode iniciar-se tanto no pós-operatório imediato quanto tardiamente.
Outras causas de transplante endotelial são responsáveis por 12,3% dos casos nos EUA, correspondendo a falências pós-transplantes penetrantes, síndrome endotelial iridocorneana e distrofia endotelial hereditária congênita. O retransplante endotelial ocorre em 8,5%. Menos comumente pode ser indicado para controle apenas da dor ou da aparência cosmética em ceratopatia bolhosa dolorosa sem prognóstico visual.5
A ideia de realizar a substituição seletiva das camadas da córnea doente é creditado a von Hippel em 1886. O primeiro transplante de córnea em que se obteve sucesso foi realizado por Zirm somente em 1905.7 Durante várias décadas os transplantes lamelares foram abandonados em favor dos transplantes penetrantes. Em 1956, Tillett realizou um transplante com característica de lamelar posterior, fazendo uma dissecção lamelar profunda da córnea receptora e utilizando suturas para fixar o enxerto doador, o que tornava o procedimento de elevada complexidade e com elevada taxa de complicações como glaucoma de fechamento angular devido a sinéquias e falência endotelial.8 Melles, em 1998, propôs então a utilização de bolha de ar em vez de suturas para fixação do enxerto, iniciando a era da moderna cirurgia endotelial nomeando-a ceratoplastia lamelar posterior. Porém, a dissecção da córnea doadora e receptora ainda era um desafio. Terry fez modificações na técnica com a introdução de novos instrumentos, utilização de câmara artificial e viscoelástico coesivo, renomeando como ceratoplastia lamelar profunda.5 Apesar disso, as técnicas não se tornaram populares devido à complexidade e à limitada acuidade visual obtida decorrente da interface gerada por duas superfícies dissecadas manualmente.9 Em 2004, Melles divulgou a técnica do stripping (retirada) da membrana de Descemet, o que evitava a manobra de dissecção estromal profunda, gerando uma superfície mais lisa para manter contato com a córnea doadora, nomeando-a Descemet Striping Endothelial Keratoplasty (DSEK). Gorovoy, em 2006, propôs a utilização do microcerátomo, facilitando o preparo do enxerto doador, denominando-a Descemet Stripping Automated Endothelial Keratoplasty (DSAEK).3 Em 2006, Melles apresentou a técnica Descemet Membrane Endotelial Keratoplasty (DMEK) experimentalmente, em que apenas endotélio e Descemet eram transplantados, com uma superfície teoricamente mais lisa do que com a presença de estroma residual como nas técnicas DSEK e DSAEK.9 Tappin mostrou que tal técnica poderia ser realizada na prática clínica, usando uma cánula para implante do enxerto conhecido como Tencell (True Endothelial Cell) (figura 4).10
2. METODOLOGIA
Análise descritiva das técnicas utilizadas para transplante endotelial, enfatizando resultados visuais obtidos e peculiaridades.
3. RESULTADOS
O número de transplantes endoteliais vem aumentando a cada ano com a transição do transplante penetrante para os lamelares. Em 2005, apenas 1429 transplantes endoteliais foram realizados, aumentando para 18221 em 2009, representando 30,5% dos transplantes realizados nos Estados Unidos (EUA). Apenas entre 2007 e 2008 esse número triplicou.3 Os transplantes penetrantes diminuíram de 45821 em 2005 para 23269 em 2009.6 Em 2011, o número de transplantes endoteliais superou o de penetrantes nos EUA.5 Aproximadamente 25000 cirurgias são realizadas por ano devido a doenças endoteliais, correspondendo a 57% das indicações de transplante.3 Foram realizados 14696 transplantes de córnea no Brasil em 2011.11 Não há dados a respeito do número de transplantes lamelares realizados.
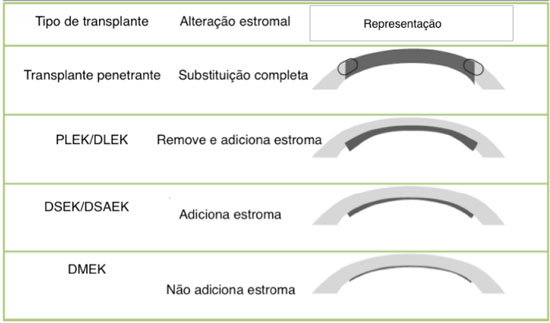
Existem na atualidade três técnicas principais para realização de transplante endotelial: DSEK, DSAEK e DMEK. As duas primeiras técnicas diferem quanto ao modo de preparo, porém as técnicas de inserção, posicionamento e fixação são semelhantes. A terceira técnica possui características próprias de preparo, inserção, posicionamento e fixação. A técnica DSEK encontra-se em desuso devido à dificuldade de execução, porém tem um custo operacional mais baixo do que o DSAEK devido ao uso de espátulas em vez do microcerátomo. A córnea doadora é montada em câmara artificial, necessitando assim de rima escleral de pelo menos 2 milímetros (mm). Com as espátulas realiza-se a dissecção do estroma profundo da córnea. A dissecção tende a ser a mais profunda possível. Na técnica DSAEK utiliza-se microcerátomo para confecção do enxerto doador, facilitando o procedimento. A córnea pode ser dissecada em duas passadas do microcerátomo, produzindo enxertos mais finos como proposto por Busin. A utilização de paquímetro ultrassônico antes da confecção do enxerto pode auxiliar na escolha da espessura da cabeça do microcerátomo que será utilizado. Além disso, o uso da tomografia de coerência óptica (OCT) previamente também pode auxiliar na escolha da cabeça do microcerátomo.
A técnica do DMEK descrita originalmente por Melles é essencialmente manual, tornando a curva de aprendizado mais longa. É realizado stripping da membrana de Descemet em 360 graus ao nível da linha de Schwalbe.(19) Para localização da membrana pode-se utilizar como referência a pigmentação do trabeculado.20 Tal manobra libera a área de maior adesão do complexo endotélio-Descemet. O importante nesse passo é garantir que não existam áreas do complexo presas à linha de Schwalbe, minimizando os riscos de rasgadura. Para facilitar a visualização do enxerto utiliza-se azul de Tripan. Em seguida tal complexo é dissecado em direção ao centro da córnea com auxílio de pinças. Essa dissecção inicial é realizada até em torno de 4 mm do centro da córnea, não necessitando abranger os 360 graus da mesma. Realiza-se trepanação parcial da área central em torno de oito milímetros de diâmetro, variando conforme o caso, evitando-se trepanação total e garantindo separação completa entre a área trepanada centralmente e a periferia. Isso é importante também para evitar rasgadura durante o preparo do enxerto. Conclui-se o stripping da Descemet, mantendo-se a córnea doadora recoberta por solução salina balanceada (BSS), diminuindo a tensão superficial, evitando o rasgo do enxerto.20 Tal técnica de manter recoberto o enxerto doador é conhecida como Scuba (Submerged Cornea Using Backgrounds Away) technique.22 Forma-se assim o enxerto doador que devido a propriedades elásticas tende a manter-se na forma de um papiro, com a face endotelial enrolando-se para dentro.
As técnicas de transplante endotelial têm proporcionado a utilização de córneas inviáveis para penetrante, como aquelas com leucomas anteriores, córneas submetidas a cirurgia refrativa, córneas de crianças e recém nascidos, etc.(4) Armou et al. encontraram taxas semelhantes de densidade endotelial entre córneas com ou sem alterações da porção anterior. Na atualidade, vem ocorrendo um aumento pela demanda de tecidos para transplante. Esse aumento vem acompanhado por um número crescente de potenciais doadores de córnea que estão sendo submetidos a cirurgia refrativa na atualidade. Com o transplante endotelial as córneas desses pacientes também podem ser captadas para transplante. Uma preocupação com a utilização dessas córneas é que as alterações observadas na porção anterior possam ser transmitidas durante a dissecção para o enxerto receptor, bem como alterações topográficas de pacientes submetidos a cirurgia refrativa. Mesmo que tais situações ocorram, pouca influência sobre a acuidade visual parece ocorrer.
Casos extremos também vêm sendo beneficiados com essas técnicas: olhos vitrectomizados, com aniridia ou submetidos a várias cirurgias fistulantes. Nessas situações, existe um maior risco de descolamento do enxerto e uma maior perda endotelial.26 Uma técnica para auxiliar em tais situações é o uso de suturas de prolene para fixação do enxerto doador.( Existem relatos de sucesso também em olhos com anomalias do desenvolvimento do segmento anterior como: Congenital hereditary endothelial distrofy (CHED), microcórnea, olhos buftálmicos, síndrome de Peters, etc. Devido aos bons resultados, a indicação cirúrgica tem sido realizada cada vez mais cedo para evitar-se ambliopia e opacificação da córnea. Nos casos de síndrome de Peters tem-se uma maior dificuldade devido a sinéquias irido-corneanas, dificultando o stripping da Descemet e a adesão do enxerto doador.31 Além disso, pacientes submetidos a transplante penetrante e que se apresentam com falência endotelial podem também ser submetidos a transplante endotelial. Falência endotelial tem sido atualmente umas das principais indicações para retransplante penetrante, perfazendo um total de 18 a 40% das indicações. As taxas de descolamento do enxerto e de perda endotelial são mais altas do que em olhos não submetidos a transplante prévio.32 Nesses casos o stripping da membrana de Descemet do receptor pode não ser realizado, já que pode ocorrer deiscência do enxerto durante as manobras. Há relato também do uso de enxertos endoteliais em casos de iminência de perfurações corneanas, promovendo suporte tectônico até completa recuperação da área de fragilidade (descemetocele).34
Dirisamer descreveu alguns casos em que houve descolamento do enxerto endotelial, porém a córnea recuperou a transparência. Tal descolamento ocorreu dentro de poucas horas após o transplante, o que suscita o questionamento se o pouco tempo de aposição entre as estruturas seria suficiente para promover repovoamento endotelial ou se esse ocorreria por um possível estímulo para multiplicação de células endoteliais. Esses casos foram englobados com o nome DMET (Descemet Membrane Endotelial Transfer).35 Três situações podem ser elencadas na situação em que houve o clareamento da córnea sem a apropriada aposição do enxerto. A primeira é de que a descemetorrexis tenha sido incompleta e que essa porção residual tenha sido capaz de promover clareamento da córnea. O segundo e terceiro cenários podem relacionar-se com a migração de células do enxerto doador para o estroma receptor e com um possível estímulo de células-tronco endoteliais.35 Outro ponto a considerar é a divisão em dois grupos: aqueles com disfunção das células endoteliais, cujo representante principal é a distrofia endotelial de Fuchs e aqueles com lesão permanente, cujo principal representante é a ceratopatia bolhosa pseudofácica. No primeiro grupo essa disfunção endotelial pode ser compensada com a retirada do tecido doente, o que estimularia a recuperação do endotélio residual. Existem relatos de que somente a descemetorrexis, sem a inserção do endotélio doador, seria estímulo suficiente para recuperação endotelial. Já no grupo da lesão endotelial permanente, para que ocorra recuperação corneana é necessário o transplante de endotélio. A principal desvantagem dessa técnica é a imprevisibilidade da recuperação endotelial e a baixa contagem endotelial obtida.35
Complicações como bloqueio pupilar (evitado com a realização de iridectomia), descolamento ou descentração do enxerto e rejeição podem ocorrer com as técnicas de transplante endotelial.16 A taxa de descolamento varia bastante (entre 1% e 82%), porém em média está abaixo de 3%.5 No caso do DMEK essas taxas também variam bastante juntamente com as taxas de rebubbling, pois pequenos descolamentos dos enxertos eram tratados de maneira diferentes: alguns cirurgiões optam por tratar sempre qualquer descolamento, enquanto outros apenas acompanham tal quadro. As taxas de rejeição no DSAEK/DSEK variam entre as séries, de 0% a 46%, entretanto a taxa média é de 10%.5 Anshu et al. conduziram um estudo comparativo sobre as taxas de rejeição entre as técnicas DMEK, DSEK/DSAEK e transplante penetrante. A incidência de episódios de rejeição foi 0,7%, 9% e 17% respectivamente. Dessa forma, com a técnica DMEK havia 15 vezes menos chance de rejeição do que com a técnica DSEK e 20 vezes a menos do que com o transplante penetrante.20 A falência primária do enxerto é outra possível complicação. Nos transplantes penetrantes ela varia de menos de 1% a 3%. Com a técnica DSEK/DSAEK ela varia entre 0 e 29%, sugerindo que o trauma cirúrgico pode ser um dos principais responsáveis pela falência. Essa taxa tende a diminuir com o aumento da experiência dos cirurgiões. Price descreveu no DMEK uma taxa de falência primária de 8% na série inicial de 60 olhos e Dapena relatou 11 falências (9,2%) em uma série de 120 olhos.8 A perda endotelial nos primeiros meses tende a ser maior com as técnicas de transplante endotelial, igualando-se em seguida à do penetrante. A média de perda endotelial entre as técnicas DSEK e DMEK é semelhante em 6 meses e 1 ano (perda endotelial de 36%).20 Por fim, o glaucoma secundário pode ocorrer com taxas variando de 0 a 54%. A etiologia inclui fechamento angular, inflamação e glaucoma cortisônico.13
DISCUSSÃO
Dessa forma, os recentes avanços nas técnicas de cirurgia de córnea têm levado ao aumento do número de ceratoplastias lamelares em relação às penetrantes. A substituição seletiva apenas da camada comprometida da córnea permite manter a integridade do bulbo ocular, tanto durante como após o procedimento cirúrgico. Doenças afetando as camadas anteriores da córnea podem ser tratadas por técnicas de transplante lamelar anterior profundo, nas quais todo o estroma é removido, mantendo a membrana de Descemet e o endotélio saudáveis. No caso das doenças endoteliais ocorre substituição seletiva apenas desta camada.37
As vantagens dos transplantes endoteliais são: realização do procedimento cirúrgico em sistema fechado, recuperação visual mais rápida, menor indução de astigmatismo, menor incidência de complicações relacionadas à sutura, preservação da estrutura corneana e diminuição da incidência de rejeição devido a menor carga antigênica. Outra possível vantagem é a utilização de uma mesma córnea para dois receptores, um que será submetido a Deep Anterior Lamellar Keratoplasty (DALK) e outro a Descemet Membrane Endothelial Keratoplasty (DMEK). Como desvantagens tem-se uma curva de aprendizado mais longa, investimento financeiro maior do que nos transplantes penetrantes, principalmente tratando-se da técnica Descemet Stripping Automated Endothelial Keratoplasty (DSAEK) e alguns resultados visuais insatisfatórios, mesmo com sucesso anatômico do transplante.7
Quando se trata apenas da técnica DMEK, outras vantagens podem ser encontradas além das citadas anteriormente: menor indução de aberrações de alta ordem, custo mais reduzido e substituição apenas da camada corneana de interesse, sem introduzir outros componentes (como o estroma). Isso torna o procedimento opticamente neutro. As desvantagens deste tipo específico de técnica são o número reduzido de cirurgiões treinados, posicionamento do paciente no pós-operatório, grande necessidade de rebubbling, necessitando atenção pós-operatória mais intensa.10 A maioria dos pacientes submetidos a DSEK/DSAEK atinge acuidade visual de 0.5, mas apenas 10 a 25% podem atingir 0.8 ou melhor. Ao contrário, 75% dos pacientes submetidos a DMEK atingem acuidade visual de 0.8 ou melhor dentro dos primeiros 6 meses após a cirurgia.38
O grande desafio das técnicas de DSEK/DSAEK, entretanto, é entender porque transplantes com sucesso anatômico excelente podem ter resultado funcional insatisfatório. É difícil estratificar a influência de variáveis confundidoras que podem também estar relacionadas com tal resultado, como por exemplo, condições oculares prévias ao transplante (doença retiniana, glaucoma, opacidade, etc.). Vários fatores podem afetar a qualidade visual em olhos submetidos a ceratoplastia. Fatores relacionados à superfície ocular e ao segmento anterior incluindo a dinâmica do filme lacrimal, aberrações corneanas de baixa e alta ordem, opacidades anteriores ou posteriores e descentrações pupilares podem ser responsáveis por resultado visual insatisfatório.40 Dirisamer et al. avaliaram as possíveis causas de baixa acuidade visual em pacientes submetidos a DMEK após acuidade visual insatisfatória com a técnica DSEK. Entre as explicações estão: falência tardia do enxerto, descolamento do mesmo, perpetuando quadro de edema estromal, refletividade aumentada na interface estromal na técnica DSEK/DSAEK, observada tanto biomicroscopicamente como com a microscopia confocal. Enquanto na técnica DMEK observa-se refletividade normal, nas outras técnicas foi observado algum grau de opacificação em 75% dos casos. Uma outra variável observada é a irregularidade na espessura do enxerto. A presença de ondulações na porção estromal interfere na qualidade óptica, já que a transparência corneana depende da interferência construtiva da luz e qualquer distorção do paralelismo das camadas estromais pode comprometer a qualidade óptica. Por fim, a presença de Descemet residual no receptor na região do eixo pupilar pode influenciar também na qualidade óptica.
Resumidamente, os dois principais fatores envolvidos nas diferenças visuais entre as técnicas DMEK e DSEK/DSAEK são a eliminação da interface estromal na primeira técnica e pelo fato de a técnica produzir um enxerto extremamente fino. Entretanto, a premissa de que a arquitetura da interface é o fator determinante na acuidade visual final pode ser confirmada quando enxertos aparentemente sem alterações anatômicas são substituídos por outro (mesmo mais espesso) e a acuidade visual melhora.
A espessura do enxerto pode ter influência na acuidade visual nos seus extremos, mas não na faixa comumente obtida (100-200 micrômetros). Não está, portanto, muito claro se tecidos mais finos proporcionam melhor visão. Na realidade a presença de qualquer interface estromal pode interferir com a visão de tal forma que a espessura não seria o ponto principal.16 Dissecção de enxertos muito finos pode, portanto, ser desnecessária.
Em pacientes submetidos a DSEK/DSAEK não ocorre compensação entre as aberrações da superfície anterior e posterior da córnea, devido à perda do paralelismo. Nos transplantes penetrantes e lamelares anteriores profundos essa compensação é mantida. Nos endoteliais com estroma residual, além de não ocorrer compensação de aberrações ópticas de alta ordem, essas podem aumentar em 20% devido à superfície posterior do transplante. Apesar disso, as irregularidades na superfície anterior da córnea seriam as principais responsáveis pela indução de aberração. A diferença nos índices de refração entre a porção anterior da córnea e o ar é maior do que a diferença entre a porção posterior da córnea e o humor aquoso, o que mais uma vez explica a importância da superfície anterior na geração de aberrações. Os aparelhos atuais possuem dificuldade em compartimentalizar a influência de cada porção da córnea nas aberrações geradas.
A superfície dos enxertos doadores pode ser outra variável que influi no resultado visual final. Enxertos mais lisos teoricamente criam uma melhor interface óptica. Com base nisso, supõe-se que a superfície corneana dissecada com microcerátomo seria mais lisa do que a dissecada com espátulas, teoricamente proporcionando uma melhor acuidade visual final.46 Isto não foi comprovado por Price, que obteve acuidade visual aos seis meses semelhante entre as técnicas DSEK e DSAEK. Na técnica DSAEK a recuperação visual foi mais rápida apenas no primeiro mês, também com menor índice de perfuração dos enxertos durante o preparo. A remodelação do estroma nos meses seguintes na técnica DSEK pode explicar a obtenção de acuidade visual semelhante aos seis meses. A média de acuidade visual após DSAEK é de 0,5, enquanto que no DSEK não é incomum obter-se 0,8, ou melhor, através de enxertos obtidos com a técnica e instrumentais corretos.
CONCLUSÃO
Assim, é de extrema importância o estímulo a pesquisas que tem como objetivo compreender a importância da interface existente nos transplantes endoteliais, buscando atingir cada vez mais uma melhor qualidade visual nesses transplantes. Com isso será possível compreender porque transplantes com resultado anatômico satisfatório não apresentam, em determinadas situações, o mesmo resultado quanto à qualidade visual.
REFERÊNCIAS
1. Kaufman PLPLA, A.; Adler, F.H. Adler's physiology of the eye. 11 ed. ed: Elsevier; 2011.
2. Dua HS, Faraj LA, Said DG, Gray T, Lowe J. Human corneal anatomy redefined: a novel pre-Descemet's layer (Dua's layer). Ophthalmology. 013;120(9):1778-85. http://dx.doi.org/10.1016/j.ophtha.2013.01.018 PMid:23714320.
3. Straiko MD, Shamie N, Terry MA. Endothelial keratoplasty: past, present, and future directions. International ophthalmology clinics. 010;50(3):123-35. http://dx.doi.org/10.1097/IIO.0b013e3181e24746 PMid:20611023.
4. Mau K. What DSAEK is going on? An alternative to penetrating keratoplasty for endothelial dysfunction. Optometry. 2009;80(9):513-23. http://dx.doi.org/10.1016/j.optm.2008.11.010 PMid:19716079.
5. Talajic JC, Straiko MD, Terry MA. Descemet's stripping automated endothelial keratoplasty: then and now. International ophthalmology clinics. 2013;53(2):1-20. http://dx.doi.org/10.1097/IIO.0b013e31827eb6ba PMid:23470585.
6. Grottone GT, Pereira NC, Gomes JA. Endothelial keratoplasty: evolution and horizons. Arquivos brasileiros de oftalmologia. 2012;75(6):439-46. http://dx.doi.org/10.1590/S0004-27492012000600016 PMid:23715152.
7. Banitt MR, Chopra V. Descemet's stripping with automated endothelial keratoplasty and glaucoma. Current opinion in ophthalmology. 2010;21(2):144-9. http://dx.doi.org/10.1097/ICU.0b013e3283360b95 PMid:20040871.
8. Anshu A, Price MO, Tan DT, Price FW, Jr. Endothelial keratoplasty: a revolution in evolution. Survey of ophthalmology. 2012;57(3):236-52. http://dx.doi.org/10.1016/j.survophthal.2011.10.005 PMid:22516537.
9. Price MO, Price FW, Jr. Endothelial keratoplasty - a review. Clinical & experimental ophthalmology. 2010;38(2):128-40. http://dx.doi.org/10.1111/j.1442-9071.2010.02213.x PMid:20398103.
10. Giebel AW. DMEK: where less is more. International ophthalmology clinics. 2013;53(1):1-14. http://dx.doi.org/10.1097/IIO.0b013e31827744c4 PMid:23221881.
11. Almeida HG, Souza ACD de. Perfil epidemiológico de pacientes na fila de transplante de córnea no estado de Pernambuco - Brasil. Rev. bras.oftalmol. 2014; 73(1): 28-32. http://dx.doi.org/10.5935/0034-7280.20140006
12. Rose L, Kelliher C, Jun AS. Endothelial keratoplasty: historical perspectives, current techniques, future directions. Canadian journal of ophthalmology Journal canadien d'ophtalmologie. 2009;44(4):401-5. http://dx.doi.org/10.3129/i09-090 PMid:19606160.
13. Dapena I, Ham L, Melles GR. Endothelial keratoplasty: DSEK/DSAEK or DMEK- the thinner the better? Current opinion in ophthalmology. 2009;20(4):299-307. http://dx.doi.org/10.1097/ICU.0b013e32832b8d18 PMid:19417653.
14. Price MO, Price FW, Jr. Descemet's stripping with endothelial keratoplasty: comparative outcomes with microkeratome-dissected and manually dissected donor tissue. Ophthalmology. 2006;113(11):1936-42. http://dx.doi.org/10.1016/j.ophtha.2006.05.034 PMid:16935344.
15. Shinton AJ, Tsatsos M, Konstantopoulos A, Goverdhan S, Elsahn AF, Anderson DF, et al. Impact of graft thickness on visual acuity after Descemet's stripping endothelial keratoplasty. The British journal of ophthalmology. 2012;96(2):246-9. http://dx.doi.org/10.1136/bjophthalmol-2011-300462 PMid:22028474.
16. Taravella MJ, Shah V, Davidson R. Ultrathin DSAEK. International ophthalmology clinics. 2013;53(2):21-30. http://dx.doi.org/10.1097/IIO.0b013e31827823a8 PMid:23470586
17. Busin M, Madi S, Santorum P, Scorcia V, Beltz J. Ultrathin descemet's stripping automated endothelial keratoplasty with the microkeratome double-pass technique: two-year outcomes. Ophthalmology. 2013;120(6):1186-94. http://dx.doi.org/10.1016/j.ophtha.2012.11.030 PMid:23466268.
18. Yoeruek E, Bayyoud T, Hofmann J, Szurman P, Bartz-Schmidt KU. Comparison of pneumatic dissection and forceps dissection in Descemet membrane endothelial keratoplasty: histological and ultrastructural findings. Cornea. 2012;31(8):920-5. http://dx.doi.org/10.1097/ICO.0b013e31823f7870 PMid:22511023.
19. Guerra FP, Anshu A, Price MO, Price FW. Endothelial keratoplasty: fellow eyes comparison of Descemet stripping automated endothelial keratoplasty and Descemet membrane endothelial keratoplasty. Cornea. 2011;30(12):1382-6. http://dx.doi.org/10.1097/ICO.0b013e31821ddd25 PMid:21993468.
20. Feng MT, Price MO, Price FW, Jr. Update on Descemet membrane endothelial keratoplasty (DMEK). International ophthalmology clinics. 2013;53(2):31-45. http://dx.doi.org/10.1097/IIO.0b013e31827822b9 PMid:23470587.
21. Tourtas T, Laaser K, Bachmann BO, Cursiefen C, Kruse FE. Descemet membrane endothelial keratoplasty versus descemet stripping automated endothelial keratoplasty. Am J Ophthalmol. 2012;153(6):1082-90.e2. http://dx.doi.org/10.1016/j.ajo.2011.12.012
22. Maier AK, Gundlach E, Gonnermann J, Klamann MK, Eulufi C, Bertelmann E, et al. Fellow Eye Comparison of Descemet Membrane Endothelial Keratoplasty and Penetrating Keratoplasty. Cornea. 2013. http://dx.doi.org/10.1097/ICO.0b013e31829dd816 PMid:23928950.
23. Armour RL, Ousley PJ, Wall J, Hoar K, Stoeger C, Terry MA. Endothelial keratoplasty using donor tissue not suitable for full-thickness penetrating keratoplasty. Cornea. 2007;26(5):515-9. PMid:17525642.
24. Phillips PM, Terry MA, Shamie N, Chen ES, Hoar KL, Stoeger C, et al. Descemet's stripping automated endothelial keratoplasty (DSAEK) using corneal donor tissue not acceptable for use in penetrating keratoplasty as a result of anterior stromal scars, pterygia, and previous corneal refractive surgical procedures. Cornea. 2009;28(8):871-6. http://dx.doi.org/10.1097/ICO.0b013e318199f8d7 PMid:19654530.
25. Moshirfar M, Khalifa YM, Davis D, Fenzl CR, Espandar L, Chang JC, et al. Descemet stripping automated endothelial keratoplasty using donor corneas with previous laser in situ keratomileusis or photorefractive keratectomy: a case series and donor cap histopathology. Cornea. 2012;31(5):533-7. http://dx.doi.org/10.1097/ICO.0b013e31820142be PMid:21993455.
26. Khor WB, Teo KY, Mehta JS, Tan DT. Descemet stripping automated endothelial keratoplasty in complex eyes: results with a donor insertion device. Cornea. 2013;32(8):1063-8. http://dx.doi.org/10.1097/ICO.0b013e31828321f8 PMid:23449486.
27. Javadi MA, Feizi S, Jafari R, Mirbabaee F, Ownagh V. Descemet Stripping Automated Endothelial Keratoplasty in Fuchs' Endothelial Dystrophy versus Pseudophakic Bullous Keratopathy. J Ophthalmic Vis Res. 2016 Oct-Dec; 11(4): 372–378. http://dx.doi.org/10.4103/2008-322X.194073. PMCID: PMC5139549.
28. Price MO, Price FW, Jr., Trespalacios R. Endothelial keratoplasty technique for aniridic aphakic eyes. Journal of cataract and refractive surgery. 2007;33(3):376-9. http://dx.doi.org/10.1016/j.jcrs.2006.10.052 PMid:17321384.
29. Busin M, Beltz J, Scorcia V. Descemet-stripping automated endothelial keratoplasty for congenital hereditary endothelial dystrophy. Archives of ophthalmology. 2011;129(9): 1140-6. http://dx.doi.org/10.1001/archophthalmol.2011.114 PMid:21555597.
30. Anwar HM, El Danasoury A, Hashem A. Descemet's stripping automated endothelial keratoplasty for congenital hereditary endothelial dystrophy. Clinical ophthalmology. 2012;6:159-63. http://dx.doi.org/10.2147/OPTH.S28405 PMid:22291459 PMCid:PMC3267538.
31. Hashemi H, Ghaffari R, Mohebi M. Posterior lamellar keratoplasty (DSAEK) in Peters anomaly. Cornea. 2012;31(10):1201-5. http://dx.doi.org/10.1097/ICO.0b013e31825697a4 PMid:22790185.
32. Covert DJ, Koenig SB. Descemet stripping and automated endothelial keratoplasty (DSAEK) in eyes with failed penetrating keratoplasty. Cornea. 2007;http://dx.doi.org/10.1097/ICO.0b013e31805fc38f26(6):692-6. PMid:17592318.
33. Straiko MD, Terry MA, Shamie N. Descemet stripping automated endothelial keratoplasty under failed penetrating keratoplasty: a surgical strategy to minimize complications. American journal of ophthalmology. 2011;151(2):233-7 e2. http://dx.doi.org/10.1016/j.ajo.2010.08.017
34. Graue-Hernandez EO, Zuniga-Gonzalez I, Hernandez-Camarena JC, Jaimes M, Chirinos-Saldana P, Navas A, et al. Tectonic DSAEK for the Management of Impending Corneal Perforation. Case reports in ophthalmological medicine. 2012;2012:916528. http://dx.doi.org/10.1155/2012/916528 PMid:23259100 PMCid:PMC3521400.
35. Dirisamer M, Ham L, Dapena I, van Dijk K, Melles GR. Descemet membrane endothelial transfer: "free-floating" donor Descemet implantation as a potential alternative to "keratoplasty". Cornea. 2012;31(2):194-7. http://dx.doi.org/10.1097/ICO.0b013e31821c9afc PMid:22146548.
36. Dirisamer M, Yeh RY, van Dijk K, Ham L, Dapena I, Melles GR. Recipient endothelium may relate to corneal clearance in descemet membrane endothelial transfer. American journal of ophthalmology. 2012;154(2):290-6 e1. DOI: http://dx.doi.org/10.1016/j.ajo.2012.02.032
37. Lim LS, Aung HT, Aung T, Tan DT. Corneal imaging with anterior segment optical c oherence tomography for lamellar keratoplasty procedures. American journal of ophthalmology. 2008;145(1):81-90. http://dx.doi.org/10.1016/j.ajo.2007.08.019 PMid:18028862.
38. Tong CM, Melles GR. Where is endothelial keratoplasty going: from Descemet stripping (automated) endothelial keratoplasty to Descemet membrane endothelial keratoplasty to Descemet membrane endothelial transfer? Canadian journal of ophthalmology Journal canadien d'ophtalmologie. 2012;47(3):197-200. http://dx.doi.org/10.1016/j.jcjo.2012.04.009 PMid:22687292.
39. Dirisamer M, Parker J, Naveiras M, Liarakos VS, Ham L, van Dijk K, et al. Identifying causes for poor visual outcome after DSEK/DSAEK following secondary DMEK in the same eye. Acta ophthalmologica. 2013;91(2):131-9. http://dx.doi.org/10.1111/j.1755-3768.2012.02504.x PMid:22989010.
40. Koh S, Maeda N, Nakagawa T, Nishida K. Quality of vision in eyes after selective lamellar keratoplasty. Cornea. 2012;31 Suppl 1:S45-9. http://dx.doi.org/10.1097/ICO.0b013e318269c9cd PMid:23038035.
41. Terry MA, Straiko MD, Goshe JM, Li JY, Davis-Boozer D. Descemet's stripping automated endothelial keratoplasty: the tenuous relationship between donor thickness and postoperative vision. Ophthalmology. 2012;119(10):1988-96. http://dx.doi.org/10.1016/j.ophtha.2012.05.021 PMid:22817831.
42. Yamaguchi T, Ohnuma K, Tomida D, Konomi K, Satake Y, Negishi K, et al. The contribution of the posterior surface to the corneal aberrations in eyes after eratoplasty. Investigative ophthalmology & visual science. 2011;52(9):6222-9. http://dx.doi.org/10.1167/iovs.11-7647 PMid:21724912.
43. Koh S, Maeda N, Nakagawa T, Higashiura R, Saika M, Mihashi T, et al. Characteristic higher-order aberrations of the anterior and posterior corneal surfaces in 3 corneal transplantation techniques. American journal of ophthalmology. 2012;153(2):284-90 e1. DOI: http://dx.doi.org/10.1016/j.ajo.2011.06.027
44. Sarayba MA, Ignacio TS, Binder PS, Tran DB. Comparative study of stromal bed quality by using mechanical, IntraLase femtosecond laser 15- and 30-kHz microkeratomes. Cornea. 2007;26(4):446-51. http://dx.doi.org/10.1097/ICO.0b013e318033e7cc PMid:17457194.
45. Marian A, Nada O, Legare F, Meunier J, Vidal F, Roy S, et al. Smoothness assessment of corneal stromal surfaces. Journal of cataract and refractive surgery. 2013;39(1):118-27. http://dx.doi.org/10.1016/j.jcrs.2012.08.050 PMid:23128030.
46. Lombardo M, De Santo MP, Lombardo G, Schiano Lomoriello D, Desiderio G, Ducoli P, et al. Surface quality of femtosecond dissected posterior human corneal stroma investigated with atomic force microscopy. Cornea. 2012;31(12):1369-75. http://dx.doi.org/10.1097/ICO.0b013e31823f774c PMid:22262224.
47. Ham L, Dapena I, van der Wees J, Melles GR. Secondary DMEK for poor visual outcome after DSEK: donor posterior stroma may limit visual acuity in endothelial keratoplasty. Cornea. 2010;29(11):1278-83. http://dx.doi.org/10.1097/ICO.0b013e3181cda01a PMid:20697285.
48. van der Meulen IJ, van Riet TC, Lapid-Gortzak R, Nieuwendaal CP, van den Berg TJ. Correlation of straylight and visual acuity in long-term follow-up of manual descemet stripping endothelial keratoplasty. Cornea. 2012;31(4):380-6. http://dx.doi.org/10.1097/ICO.0b013e31823f8ab7 PMid:22262226.



Fonte de financiamento: declaram não haver
Conflito de interesses: declaram não haver
Recebido em:
19 de Outubro de 2015.
Aceito em:
13 de Novembro de 2015.