José Maurício Botto Garcia1; Tainara Sardeiro de Santana1; David Leonardo Cruvinel Isaac2; Marcos Pereira Ávila2
DOI: 10.17545/eOftalmo/2021.0030
RESUMO
A miopia é o distúrbio ocular mais comum em todo o mundo e sua incidência está aumentando rapidamente. O termo “alta miopia” refere-se a um maior comprimento axial (tipicamente acima de 26,50 mm) e um equivalente esférico maior que −6,0 D. Em 1970, foi elaborada a primeira definição da maculopatia miópica, que incluía a presença de atrofia coriorretiniana, manchas pigmentares centrais, fissuras craqueladas, estafiloma posterior e alterações do disco óptico. O objetivo dos autores é descrever o status atual da tomografia de coerência óptica em B-scans, ajudando especialistas em retina no diagnóstico e decisão terapêutica sobre a maculopatia por tração macular. Indivíduos com alta miopia podem desenvolver várias patologias maculares, como foveosquise miópica e orifício macular, com ou sem descolamento de retina. Após avanços recentes nas técnicas de imagem, nossa compreensão da patologia macular na miopia melhorou significativamente. Novas condições foram identificadas e definidas. Os autores desejam destacar a importância da tomografia de coerência óptica no monitoramento de pacientes, usando dados publicados recentemente, a fim de alcançar os melhores resultados possíveis.
Palavras-chave: Miopia; Tomografia óptica; Macular.
ABSTRACT
Myopia is the most common ocular disorder worldwide, and its incidence is increasing rapidly. The term “high myopia” refers to a higher axial length (typically over 26.50 mm) and a spherical equivalent higher than -6.0D. In 1970, myopic maculopathy had its first definition reported, including the presence of chorioretinal atrophy; central pigment spots; lacquer cracks; posterior staphyloma; and optic disc changes. The purpose of the authors is to depict the status of optical coherence tomography B-scans helping retina specialists on diagnosis and therapeutic decision on macular traction maculopathy. Individuals with high myopia can suffer from the development of several macular pathologies, such as myopic foveoschisis, macular hole with and without retinal detachment. Recent advances in imaging techniques, our understanding of macular pathology in myopia has significantly improved. New conditions have been identified and defined. Our purpose is to highlight the importance of optical coherence tomography when monitoring patients, using recently published data, in order to achieve the best possible results.
Keywords: Myopia; Tomography optical; Macular.
INTRODUÇÃO
A miopia é o distúrbio ocular mais comum em todo o mundo e sua incidência está aumentando rapidamente. Em 2010, até 27% da população mundial eram míopes e 2,8% tinham alta miopia. Estima-se que esses números aumentem para 52% e 10%, respectivamente, até 2050. O termo “alta miopia” refere-se a um comprimento axial mais alto (tipicamente acima de 26,50 mm) e um equivalente esférico maior que −6,0 D(1,2). Em 1970, foi elaborada a primeira definição da maculopatia miópica, que incluía a presença de atrofia coriorretiniana, manchas pigmentares centrais, fissuras craqueladas, estafiloma posterior e alterações do disco óptico. Em 1984, Ávila et al. propuseram pela primeira vez sistema de classificação para descrever o curso natural da atrofia macular secundária à maculopatia miópica, com base em angiofluoresceinografia e fotografias estereoscópicas do fundo de olho(3).
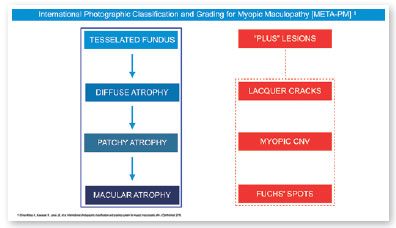
Em 2015, um painel internacional recomendou um novo sistema de estadiamento fotográfico para a maculopatia miópica, chamado classificação META–PM. Este estudo publicou dados de longo prazo sobre a progressão natural da maculopatia miópica, descrevendo os principais sinais nas seguintes categorias: ausência de alterações miópicas (categoria 0), fundo tesselado (categoria 1), atrofia coriorretiniana difusa (categoria 2), atrofia coriorretiniana irregular (categoria 3) e atrofia macular (categoria 4) (Figura 1). As lesões que se desenvolvem independentemente do padrão dominante de evolução clínica foram consideradas “lesões adicionais”, incluindo fissuras craqueladas, neovascularização coroidal miópica (NVCM) e mancha de Fuchs (fase cicatricial da NVCM) (Figura 2). Aos pacientes com lesões de categoria 2 ou mais graves, ou com lesões adicionais, foi aplicada a designação “miopia patológica”(4). No entanto, o META–PM apresentou limitações, como o fato de que a imagem do fundo pode aparecer de forma diferente conforme a raça, dependendo do grau de pigmentação do fundo, e algumas condições maculares, como a maculopatia por tração miópica (MTM) (Figura 2) e a mácula em forma de cúpula (MFC) (Figura 4) não foram incluídas(5).
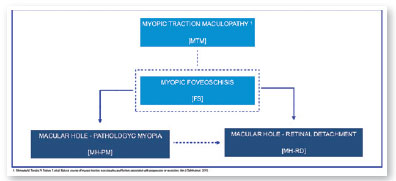
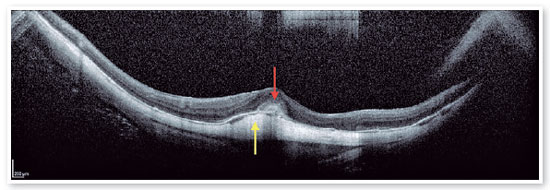
O conceito atual de MTM compreende um grande espectro de apresentações, que inclui a foveosquise miópica (FSM), uma tração macular persistente com esquise intrarretiniana, e o orifício macular de alta miopia (OM–AM), com ou sem descolamento de retina (OM–DR). Relata-se que a prevalência de MTM varia de 9% a 34,4% em pacientes altamente míopes. A tomografia de coerência óptica (OCT) é uma ferramenta não invasiva que permite a detecção e o acompanhamento de muitas complicações em pacientes com alta miopia, incluindo o estafiloma posterior (Figura 5), a MTM, o OM–AM e o OM–DR.
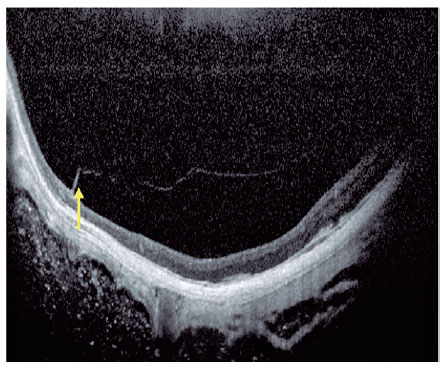
Vários avanços na tecnologia de imagem permitiram um estudo in vivo detalhado do perfil de pacientes altamente míopes. A OCT de varredura da fonte (SS–OCT) tem sido usada e identificou a diminuição da espessura da coroide (EC) como uma característica importante na atrofia macular, demonstrando que valores menores de EC têm uma associação maior com a atrofia macular miópica que a espessura da esclera(6). A angiografia por OCT mostrou que a NVCM mantém um fluxo sanguíneo detectável na fase atrófica muito tempo após seu surgimento. Na fase ativa, é claramente visível uma rede vascular, mas na fase cicatricial, a NVCM diminui de tamanho e assume um formato irregular. Na fase atrófica, ainda é possível detectar NVCM com fluxo sanguíneo(7).
O objetivo dos autores é demonstrar a importância da OCT na MTM, discutindo o momento ideal para cirurgia ou acompanhamento clínico, para alcançar os melhores resultados possíveis., descrevendo como o status atual dos exames de OCT em B-scans pode ajudar os especialistas em retina tanto no diagnóstico quanto na decisão terapêutica em casos de MTM.
MÉTODOS
Este artigo apresenta uma revisão não sistemática da literatura. Para o levantamento da literatura, foram pesquisados artigos na National Library of Medicine, compreendendo o conjunto de dados MEDLINE (PubMedTM). Os descritores utilizados foram: maculopatia de tração miópica (MTM), foveosquise miópica (FSM), orifício macular de alta miopia (OM–AM) com e sem descolamento de retina (OM–DR) e tomografia de coerência óptica (OCT). Para a seleção dos itens adequados, foram incluídos artigos particularmente relevantes sobre o assunto.
1. Foveosquise e alta miopia:
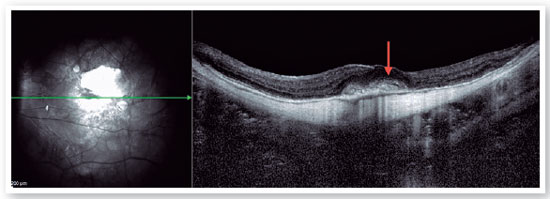
A foveosquise miópica (FSM) é uma complicação da miopia patológica ou miopia alta que coloca em risco a visão(1,8,9). A FSM é uma separação das camadas da retina na mácula que causa um acúmulo de líquido intrarretiniano e sub-retiniano na mácula, na ausência de um orifício macular de espessura total com cistos ou colunas intrarretinianas (Figura 6)(9–11). Acredita-se que um descolamento vítreo posterior incompleto ou anômalo esteja relacionado à patogênese da FSM e uma contração do vítreo cortical pode induzir essa divisão intrarretiniana. Várias complicações podem ocorrer durante a evolução da FSM, como OM–AM e OM–DR, que podem levar à perda da visão. A prevalência da FSM varia de 9 a 20% nas populações altamente míopes. Portanto, sua importância clínica não é desprezível.
O estafiloma posterior é um abaulamento posterior ou ectasia do globo ocular que pode estar presente em pacientes com alta miopia. Atualmente, entende-se que pacientes com estafiloma posterior associado a um maior comprimento axial têm um risco maior de desenvolver FSM(8,17–19). A patogênese da FSM inclui uma tração anormal pela membrana hialoide posterior, combinada com alterações anatômicas na interface vitreomacular, desencadeadas pelo contorno anormal do estafiloma posterior. O grupo de Ohno Matsui classificou esta doença em cinco categorias diferentes, com base na localização e no tamanho da área afetada, variando desde a ausência de foveosquise aparente (S0) até o acometimento macular completo (S4) (Figura 7).
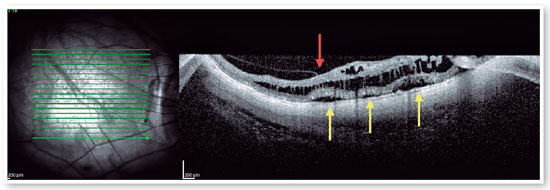
A vitrectomia via pars plana com peeling da membrana limitante interna (com ou sem tamponamento com gás) é a base para o tratamento cirúrgico da FSM(5,8). A progressão natural da FSM é, em geral, mal compreendida. A OCT de domínio espectral (SD–OCT) é extremamente útil na avaliação da FSM. A SD–OCT com B-scan pode mostrar a separação da retina neurossensorial (e subsequentemente da membrana epirretiniana) que é associada à tração vitreomacular(20). A questão de fundo é decidir com base nos achados da OCT entre indicar uma abordagem cirúrgica ou apenas acompanhar os pacientes clinicamente. Acredita-se que a FSM progrida para orifício macular lamelar ou descolamento da fóvea (DF).
O momento ideal para a cirurgia em pacientes com FSM continua controverso, mas características específicas da SD–OCT podem ajudar a decidir se a vitrectomia é a opção mais apropriada para cada paciente. Gaucher et al. revisaram retrospectivamente 29 prontuários de olhos durante até 31,2 meses. A acuidade visual piorou em 20 olhos (69%) e ficou estável em 9 olhos (31%). Observou-se o desenvolvimento de OM–AM em 9 dos 29 olhos durante o período de acompanhamento; 6 dos 9 olhos que desenvolveram OM–AM já tinham DF antes da formação do orifício. Esses mesmos autores relataram que a combinação de MTM com DF torna provável o desenvolvimento de um orifício macular de espessura total(19). Em uma série observacional de casos sobre desfechos cirúrgicos para MTM, OM–AM e OM–DR, a média da melhor acuidade visual corrigida aos 6 meses após a vitrectomia em olhos tratados para OM–DR foi significativamente pior em comparação com a média dos olhos tratados para MTM sem orifício macular. Assim, é melhor operar antes que se desenvolva um OM–DR(1,8,21,22).
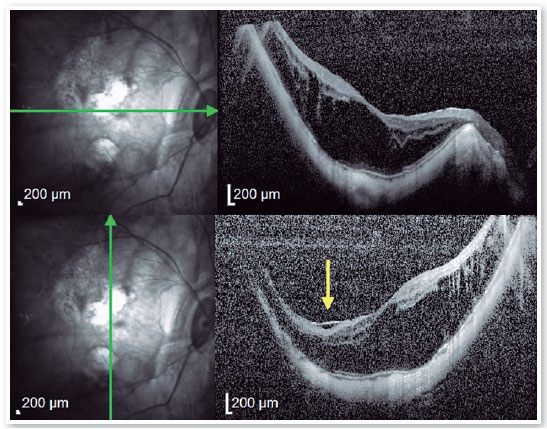
Conclui-se que pacientes com FSM devem ser monitorados regularmente quanto à existência de um DF, e deve ser considerado o tratamento cirúrgico quando ocorrer um descolamento da fóvea, visando prevenir o desenvolvimento de um orifício macular de espessura total e um subsequente OM–DR (Figuras 8 e 9). Olhos que apresentam ruptura elipsoide pré-operatória e espessura foveal central mais fina também tendem a ter desfechos visuais piores(21).
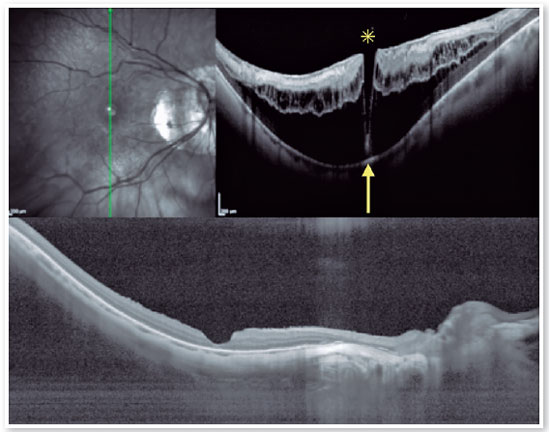
2. Orifício macular de alta miopia (OM–AM):
O OM–AM é uma complicação relativamente comum em pacientes com MTM que apresentam um comprimento axial maior que 26,5 mm ou uma refração maior que −6,00 D(1,21). Sua prevalência é de cerca de 8,4%(5). Orifícios maculares também são reconhecidos como um fator predisponente ao descolamento de retina de polo posterior(11,12,21,22). Exames de OCT em B-scan que demonstrem uma FSM estão associados a um pior prognóstico anatômico e funcional e à progressão para um estágio mais avançado enquanto uma tração persistente continuar atuando, o que pode resultar na formação de um OM–AM. A resolução espontânea da MTM com OM–AM é rara sem uma abordagem cirúrgica, mas já foi relatada(24). O desenvolvimento de um OM–AM está associado a uma tração anteroposterior e tangencial sobre a mácula, de forma intimamente relacionada ao que ocorre em olhos emetropes. No entanto, é comum que a manifestação de um estafiloma posterior, promovendo a separação das camadas da retina, associe um OM–AM a uma FSM(12,22). Shimada et al. relataram que embora 3,9% dos casos de MTM tenham desenvolvido descolamento de retina, a decisão quanto à adoção de uma abordagem cirúrgica deve ser tomada com cuidado, pois 27,3% dos casos de OM–AM ocorreram após uma cirurgia para MTM(8,23).
É difícil decidir se é necessária uma intervenção cirúrgica e se for, determinar o momento ideal da cirurgia, pois tanto a exacerbação quanto a melhora espontânea são possíveis(1,12). Foi relatado que o OM–AM com FSM teve um resultado pior que sem FSM(8,23,24). Desde a introdução da vitrectomia via pars plana de três vias com tamponamento gasoso, várias estratégias cirúrgicas foram desenvolvidas para a correção de OM–AM em pacientes com alta miopia, incluindo o tamponamento com óleo de silicone, o buckling macular posterior e supracoroidal e a técnica de encurtamento da esclera(1,12,14,15,21,25). Estudos anteriores mostraram que os procedimentos que usam óleo de silicone pesado têm uma taxa de recolocação de aproximadamente 87%, comparada a uma taxa de 53% para procedimentos com óleo de silicone padrão. No entanto, apesar da maior taxa de sucesso com o óleo pesado, não houve diferença estatisticamente significativa na visão final(12). As dificuldades técnicas inerentes ao buckling macular e o risco de lesões nas estruturas ao redor pareciam impedir que esse procedimento se tornasse comum. Mas com o passar do tempo, o buckling macular foi sendo gradualmente reconhecido como um procedimento importante para neutralizar mecanicamente os efeitos de tração do estafiloma posterior, relaxando a retina e facilitando assim o fechamento do orifício(25).
A presença de FSM indica que o estafiloma posterior desempenha um papel importante na patogênese do alongamento da retina, ao produzir uma tensão externa em um complexo vitreorretiniano interno mais rígido, incluindo uma membrana limitante interna mais rígida. Consequentemente, aliviar a tração anteroposterior e tangencial sobre a mácula por meio de uma vitrectomia combinada com a remoção da membrana limitante interna pode esticar o orifício macular, porque a retina seria forçada a se fixar no arco mais largo da parede escleral posterior profunda (Figura 10)(9,12,19,21). O OM–AM sem descolamento de retina pode ser classificado em duas categorias, com base na estrutura da fóvea: tipo esquise e tipo plano(1). A cirurgia de buckling macular pode ser benéfica para este tipo de OM–AM, mas deve-se considerar sua natureza invasiva e o possível comprometimento da circulação coroidal. Já o OM–AM sem FSM tem uma patogênese semelhante à dos orifícios maculares idiopáticos e tem resultados pós-operatórios mais favoráveis(25).
3. Orifício macular com descolamento de retina (OM–DR):
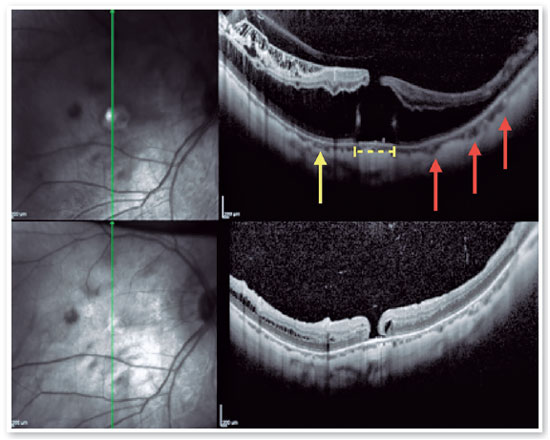
O OM–DR é uma complicação que representa uma das maiores ameaças aos olhos com alta miopia, e é relatado em cerca de 67,7% deles (Figuras 11 e 12)(26,27). Embora sua patogênese não seja completamente compreendida, o maior comprimento axial, a formação de um estafiloma posterior, a tração tangencial do córtex vítreo e a rigidez das membranas limitante interna e epirretiniana podem estar relacionados(2). Por isto, acredita-se que a vitrectomia combinada com o peeling da membrana limitante interna seja um procedimento benéfico para esses pacientes. A justificativa seria que esse procedimento aliviaria completamente a tração macular e aumentaria a flexibilidade da retina para se adaptar melhor ao estafiloma posterior(21,26,27). Foi relatado que a OCT intraoperatória afeta a decisão cirúrgica em mais de 40% dos casos, auxiliando na identificação dos locais de clivagem entre as membranas limitante interna e epirretiniana e desempenhando um papel significativo na tomada de decisão(22,26).
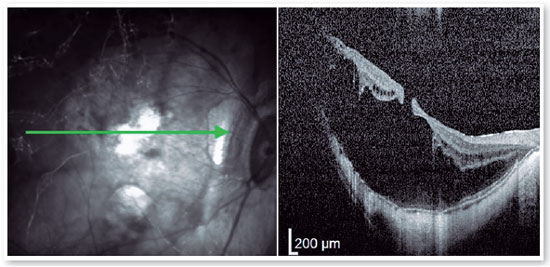
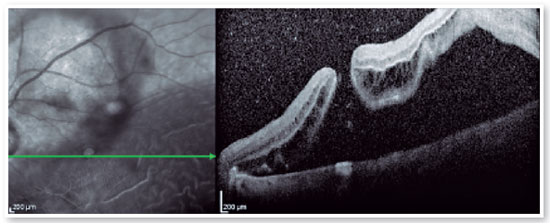
Embora o OM–DR geralmente seja tratado com cirurgia vítrea para liberar a tração vítrea ou com tamponamento de gás, seu prognóstico é ruim(27).
A abordagem cirúrgica para o OM–DR é ligeiramente diferente da cirurgia para o OM–AM sem descolamento simultâneo de retina e costuma ser mais desafiadora. O OM–DR é uma doença refratária com mau prognóstico visual. Apesar de todas as intervenções potenciais promissoras, ainda podem ocorrer a reabertura do orifício macular e o descolamento recorrente da retina, principalmente na miopia axial extremamente alta(2,15,23,27). A técnica de retalho invertido da membrana limitante interna para tratar o OM–DR tem apresentado resultados satisfatórios. O sucesso anatômico do retalho invertido no OM–AM sem descolamento de retina varia de 94% a 100%, mas relatou-se uma taxa de fechamento de 100% em pacientes com OM–DR(14,16,26,27).
4. Tratamento cirúrgico da maculopatia por tração miópica (MTM):
O principal desafio do tratamento cirúrgico da MTM é fazer o peeling da membrana limitante interna por sobre a retina descolada e móvel. O peeling da membrana limitante interna é crucial no OM–DR (ao contrário do que ocorre no OM–AM sem descolamento de retina), para que sejam liberadas todas as forças de tração. A técnica assistida por perfluorcarbono líquido (PFCL) pode ajudar a manter a retina firme e menos móvel durante o peeling da membrana limitante interna. Além disso, essa técnica proporciona uma melhor coloração antes do peeling propriamente dito. Uma pequena quantidade de PFCL é injetada no olho para cobrir o orifício macular. Verde de indocianina (ICG) ou azul brilhante G (BBG) diluído é injetado ao redor da bolha de PFCL para corar a membrana limitante interna. O PFCL impede que o corante tenha acesso ao espaço sub-retiniano. Obter uma boa coloração é fundamental para um peeling completo da membrana limitante interna. Inclinando-se o olho, pode-se espremer o corante por baixo do PFCL e por sobre a membrana limitante interna, para facilitar uma boa coloração(14,16,28,29).
Para evitar complicações resultantes de trauma iatrogênico, foram desenvolvidas pinças de haste longa para peeling da membrana limitante interna, específicas para olhos com alta miopia. Foram desenvolvidas pinças de calibre 27+ com uma plataforma de preensão distendida e uma área quase igual à das pinças de calibre 25+. Essas pinças são 59% maiores que a plataforma anterior de calibre 27; portanto, reduzem proporcionalmente a pressão na membrana e minimizam a probabilidade de a membrana ser rasgada por uma pressão excessiva. A pinça 27+ apresenta a mesma plataforma de preensão conformante das versões de calibres 23 e 25+, com um formato mais retangular. Isso pode reduzir o risco de preensão da camada de fibras nervosas da retina pela borda da plataforma de preensão, o que poderia ocorrer com uma configuração mais angular. Com relação à membrana limitante interna, a técnica de pinçar e destacar pode funcionar melhor para iniciar o peeling em uma retina descolada e móvel(12,24,28,29).
A cirurgia de buckling macular é uma alternativa de abordagem para tratar casos recorrentes ou difíceis de OM–DR. Essa cirurgia ajuda no fechamento do orifício ao inserir uma crista que empurra toda a mácula para frente. Isso poderia explicar por que os olhos míopes com orifícios maculares e MFC são menos suscetíveis ao descolamento de retina: assim como ocorre em olhos com buckle macular implantado, a MFC reduz a curvatura do estafiloma e pode impedir o descolamento da retina(19,25). Nesse sentido, alguns autores relataram melhores resultados com o buckling macular que com a vitrectomia, mesmo em casos de OM–DR primário. Relatos recentes sugerem que a combinação de buckling macular e vitrectomia com peeling da membrana limitante interna pode ser uma alternativa promissora em casos refratários(25,29).
Indivíduos com alta miopia podem sofrer com o desenvolvimento de várias patologias maculares, como a FSM, o OM–AM e o OM–DR. Com os recentes avanços nas técnicas de imagem, como a SD-OCT e a SS-OCT, nossa compreensão da patologia macular na miopia melhorou significativamente. Novas condições, como a MTM, foram identificadas e definidas. O momento ideal para a cirurgia em pacientes com FSM permanece controverso, mas características específicas da SD–OCT podem ajudar a decidir se a vitrectomia é a opção mais apropriada para o paciente. Portanto, pacientes com FSM devem ser monitorados regularmente quanto ao descolamento da fóvea e o tratamento cirúrgico deve ser considerado quando se desenvolver esse descolamento. Relata-se ocasionalmente uma rápida progressão da MTM devida a uma FSM grave para um descolamento da fóvea ou um micro-orifício macular, mesmo quando o período de espera para a cirurgia foi curto, como recomendado após cuidadosa deliberação com base em imagens de OCT em B-scans. As abordagens de tratamento agora estão sendo planejadas com base nas características patológicas e anatômicas da MTM, tais como visualizadas na OCT. Propõe-se que o melhor momento para realizar uma vitrectomia para FSM é quando a acuidade visual começa a piorar, antes do aparecimento do descolamento da fóvea ou no momento de seu diagnóstico. É importante destacar a importância da OCT durante o acompanhamento dos pacientes diagnosticados com MTM, visando alcançar os melhores resultados possíveis. Assim, a avaliação por OCT após a cirurgia também é recomendada.
REFERÊNCIAS
1. Gómez-Resa M, Burés-Jelstrup A, Mateo C. Myopic traction maculopathy. Dev Ophthalmol. 2014;54:204-12.
2. Hashimoto S, Yasuda M, Fujiwara K, Ueda E, Hata J, Hirakawa Y, et al. Association between Axial Length and Myopic Maculopathy: The Hisayama Study. Ophthalmol Retina. 2019;3(10):867-73.
3. Avila MP, Weiter JJ, Jalkh AE, Trempe CL, Pruett RC, Schepens CL. Natural history of choroidal neovascularization in degenerative myopia. Ophthalmology. 1984;91(12):1573-81.
4. Ohno-Matsui K, Kawasaki R, Jonas JB, Cheung CMG, Saw SM, Verhoeven VJM, Klaver CCW, Moriyama M, Shinohara K, Kawasaki Y, Yamazaki M, Meuer S, Ishibashi T, Yasuda M, Yamashita H, Sugano A, Wang JJ, Mitchell P, Wong TY, META-analysis for Pathologic Myopia (META-PM) Study Group. International photographic classification and grading system for myopic maculopathy. Am J Ophthalmol. 2015;159(5):877-83.e7.
5. Ruiz-Medrano J, Montero JA, Flores-Moreno I, Arias L, García-Layana A, Ruiz-Moreno JM. Myopic maculopathy: Current status and proposal for a new classification and grading system (ATN). Prog Retin Eye Res. 2019 Mar;69:80-115.
6. Wong CW, Teo YCK, Tsai STA, Ting SWD, Yeo YSI, Wong WKD, et al. Characterization of the choroidal vasculature in myopic maculopathy with optical coherence tomographic angiography. Retina. 2019;39(9):1742-50.
7. Ishida T, Watanabe T, Yokoi T, Shinohara K, Ohno-Matsui K. Possible connection of short posterior ciliary arteries to choroidal neovascularisations in eyes with pathologic myopia. Br J Ophthalmol. 2019;103(4):457-62.
8. Shimada N, Ohno-Matsui K, Baba T, Futagami S, Tokoro T, Mochizuki M. Natural course of macular retinoschisis in highly myopic eyes without macular hole or retinal detachment. Am J Ophthalmol. 2006;142(3):497-500.
9. Steel DH, Lotery AJ. Idiopathic vitreomacular traction and macular hole: a comprehensive review of pathophysiology, diagnosis, and treatment. Eye (Lond). 2013;27 Suppl 1(Suppl 1):S1-21.
10. Brockmann T, Steger C, Weger M, Wedrich A, Haas A. Risk assessment of idiopathic macular holes undergoing vitrectomy with dye-assisted internal limiting membrane peeling. Retina. 2013;33(6):1132-6.
11. Casuso LA, Scott IU, Flynn HW Jr., Gass JD, Smiddy WE, Lewis ML, et al. Long-term follow-up of unoperated macular holes. Ophthalmology. 2001;108(6):1150-5.
12. De Giacinto C, Pastore MR, Cirigliano G, Tognetto D. Macular Hole in Myopic Eyes: A Narrative Review of the Current Surgical Techniques. J Ophthalmol. 2019 Mar 11;2019:3230695.
13. Madi HA, Masri I, Steel DH. Optimal management of idiopathic macular holes. Clin Ophthalmol. 2016 Jan 13;10:97-116.
14. Michalewska Z, Michalewski J, Dulczewska-Cichecka K, Nawrocki J. Inverted internal limiting membrane flap technique for surgical repair of myopic macular holes. Retina. 2014; 34(4):664-9.
15. Morescalchi F, Costagliola C, Gambicorti E, Duse S, Romano MR, Semeraro F. Controversies over the role of internal limiting membrane peeling during vitrectomy in macular hole surgery. Surv Ophthalmol. 2017;62(1):58-69.
16. Oleñik A, Rios J, Mateo C. Inverted internal limiting membrane flap technique for macular holes in high myopia with axial length ≥30 mm. Retina. 2016;36(9):1688-93.
17. Curtin BJ, Karlin DB. Axial length measurements and fundus changes of the myopic eye. Am J Ophthalmol. 1971;71(1 Pt 1):42-53.
18. Dai F, Li S, Wang Y, li S, Han J, Li M, et al. Correlation between posterior staphyloma and dome-shaped macula in high myopic eyes. Retina. 2020;40(11):2119-26.
19. Gaucher D, Erginay A, Lecleire-Collet A, Haouchine B, Puech M, Cohen SY, et al. Dome-shaped macula in eyes with myopic posterior staphyloma. Am J Ophthalmol. 2008;145(5):909-14.
20. Fang Y, Du R, Nagaoka N, Yokoi T, Shinohara K, Xu X, et al. OCT-Based Diagnostic Criteria for Different Stages of Myopic Maculopathy. Ophthalmology. 2019;126(7):1018-32.
21. Lim LS, Ng WY, Wong D, Wong E, Yeo I, Ang CL, et al. Prognostic factor analysis of vitrectomy for myopic foveoschisis. Br J Ophthalmol. 2015;99(12):1639-43.
22. Gohil R, Sivaprasad S, Han LT, Mathew R, Kiousis G, Yang Y. Myopic foveoschisis: a clinical review. Eye (Lond). 2015;29(5):593-601.
23. Shimada N, Tanaka Y, Tokoro T, Ohno-Matsui K. Natural course of myopic traction maculopathy and factors associated with progression or resolution. Am J Ophthalmol. 2013;156(5):948-57.e1.
24. Ono T, Terada Y, Mori Y, Kataoka Y, Nakahara M, Miyata K. Spontaneous resolution of myopic foveoschisis and a macular hole with retinal detachment. Am J Ophthalmol Case Rep. 2019 Jan 9;13:143-6.
25. Alkabes M, Mateo C. Macular buckle technique in myopic traction maculopathy: a 16-year review of the literature and a comparison with vitreous surgery. Graefes Arch Clin Exp Ophthalmol. 2018;256(5):863-77.
26. Gao X, Guo J, Meng X, Wang J, Peng X, Ikuno Y. A meta-analysis of vitrectomy with or without internal limiting membrane peeling for macular hole retinal detachment in the highly myopic eyes. BMC Ophthalmol. 2016 Jun 13;16:87.
27. Yuan J, Zhang LL, Lu YJ, Han MY, Yu AH, Cai XJ. Vitrectomy with internal limiting membrane peeling versus inverted internal limiting membrane flap technique for macular hole-induced retinal detachment: a systematic review of literature and meta-analysis. BMC Ophthalmol. 2017;17(1):219.
28. Andrew N, Chan WO, Tan M, Ebneter A, Gilhotra JS. Modification of the Inverted Internal Limiting Membrane Flap Technique for the Treatment of Chronic and Large Macular Holes. Retina. 2016;36(4):834-7.
29. Chen SN, Yang CM. Inverted Internal Limiting Membrane Insertion for Macular Hole-Associated Retinal Detachment in High Myopia. Am J Ophthalmol. 2016 Feb;162:99-106.e1.
INFORMAÇÃO DOS AUTORES

Financiamento: Declaram não haver
Conflitos de Interesse: Declaram não haver
Recebido em:
13 de Novembro de 2020.
Aceito em:
14 de Outubro de 2021.