Aline Mota Freitas Matos1; Gustavo Henrique de Lima Melillo2; Bianca Figueiredo Barczewski3
DOI: 10.17545/eoftalmo/2018.0033
RESUMO
A histiocitose de células de Langerhans (LCH) abrange um grupo de desordens caracterizadas pela proliferação clonal e acúmulo dessas células em vários órgãos como pele, tecidos hematopoiéticos ou linfóides, pulmões, fígado, hipotálamo e ossos. A apresentação de lesão palpebral é extremamente rara. Aqui, relatamos um caso de LCH de pálpebra superior limitada à pele. Uma paciente de 35 anos apresentou um nódulo sólido com crosta na margem da pálpebra superior esquerda, causando mal direcionamento de alguns dos cílios adjacentes com crescimento progressivo durante um ano. Biópsia excisional foi realizada e a análise histológica revelou histiócitos com citoplasma eosinofílico, positividade imunoistoquímica para S-100, laminina e CD1a, revelando LCH. Embora rara, a LCH limitada à pele deve ser incluída nos diagnósticos diferenciais de lesões tumorais palpebrais.
Palavras-chave: Histiocitosis; Pálpebras; Células de Langerhans.
ABSTRACT
The Langerhans’ Cell Histiocytosis (LCH) is a group of disorders caused by clonal proliferation and accumulation of these cells in various organs, such as skin, hematopoietic or lymphoid tissues, lungs, liver, hypothalamus and bones. The eyelid presentation is extremely rare. Here, we report a case of a skin-limited upper eyelid LCH. The 35-year-old woman presented solid crusted nodule on the left upper eyelid margin, causing the misdirection of some of the adjacent eyelashes with progressive growth for 1 year. Excisional biopsy was performed, and histological analysis revealed histiocytes with eosinophilic cytoplasm, immunohistochemical positivity for S-100, laminin and CD1a, which showed LCH. Though rare, the skin-limited LCH should be included in the differential diagnoses of tumoral lesions of the eyelid.
Keywords: Histiocytosis; Eyelid; Langerhans Cells.
RESUMEN
La histiocitosis de células de Langerhans (HCL) abarca un grupo de desórdenes caracterizados por la proliferación clonal y acúmulo de dichas células en varios órganos, como piel, tejidos hematopoyético o linfoide, pulmones, hígado, hipotálamo y huesos. La presentación de lesión palpebral es extremadamente rara. Aquí, relatamos un caso de HCL de párpado superior limitada a la piel. Una paciente de 35 años presentó un nódulo sólido con costra en el margen del párpado superior izquierdo, causando mal direccionamiento de algunas de las pestañas adyacentes con crecimiento progresivo durante un año. Se ha realizado la biopsia excisional y el análisis histológico ha indicado histiocitos con citoplasma eosinófilo, positividad inmunohistoquímica para S-100, laminina y CD1a, indicando HCL. Aunque rara, la HCL limitada a la piel debe incluirse en los diagnósticos diferenciales de lesiones tumorales palpebrales.
Palabras-clave: Histiocitose; Párpados; Células de Langerhans.
INTRODUÇÃO
A histiocitose é caracterizada como lesões proliferativas compostas de macrófagos e células dendríticas e pode causar uma ampla gama de distúrbios sistêmicos. As células de Langerhans são um tipo imaturo de células dendríticas tipicamente presentes na pele e mucosa que desempenham um papel importante nas respostas imunes1. A histiocitose de células de Langerhans (LCH), também denominada histiocitose X, é caracterizada por um grupo de distúrbios causados pela proliferação clonal e acúmulo dessas células em vários órgãos como pele, tecidos hematopoiéticos ou linfóides, pulmões, fígado, hipotálamo e ossos. Tipicamente descrito em crianças, seu curso varia de involução espontânea benigna a insuficiência sistêmica2. Casos de apresentação palpebral têm sido raramente relatados, poucos deles em adultos3. Apresentamos aqui um caso deste diagnóstico incomum de margem palpebral.
RELATO DE CASO
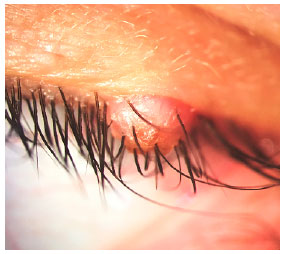
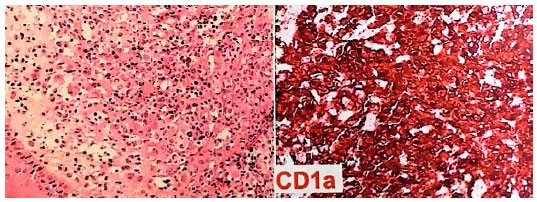
Uma paciente de 35 anos apresentou um nódulo sólido com crosta na margem da pálpebra superior esquerda (Figura 1), causando mal direcionamento de alguns dos cílios adjacentes. A lesão vinha crescendo há 1 ano. A paciente negou outras lesões semelhantes no corpo e, com exceção do hipotireoidismo, não relatou nenhum antecedente pessoal ou familiar relevante. A BCVA foi de 20/20 em ambos os olhos. Os resultados de outros exames oftalmológicos estavam dentro dos limites normais. Biópsia excisional foi realizada. A análise anatomopatológica revelou histiócitos com citoplasma eosinofílico, positividade imunoistoquímica para S-100, laminina e mais notadamente para CD1a (Figura 2). Diante desses achados, um diagnóstico de LCH foi feito.
DISCUSSÃO
Os histiócitos são células do sistema reticuloendotelial e incluem macrófagos, células dendríticas e células de Langerhans (LC). As LC são geralmente caracterizadas pela presença de grânulos de Birbeck, organelas supostamente envolvidas na internalização de antígenos4. As LC geralmente ocorrem na superfície do corpo, como epiderme, conjuntiva e limbo corneal. Elas são raras na conjuntiva tarsal saudável. No entanto, as LC são numerosas no tecido subconjuntival e na pele da margem palpebral de pacientes com conjuntivite alérgica5.
As lesões nodulares da pálpebra estão entre as anormalidades mais freqüentes da área periocular. A base dos cílios é um local comum para a presença de hidrocistoma écrino, calázio, cisto sebáceo, siringoma, xantelasma, cisto de inclusão epidérmica e tumores malignos. O diagnóstico diferencial é fundamental para o tratamento e acompanhamento corretos e é feito tanto clínica como histologicamente. No entanto, a LCH raramente é localizada neste sítio. Não encontramos mais de 6 relatos de casos de tumor palpebral, e apenas 1 deles estava na pálpebra superior3,4,6-9.
A LCH foi descrita pela primeira vez em 1893 por Alfred Hand Jr., que observou exoftalmia, hepatoesplenomegalia, linfadenopatia e diabetes insípido. Ao longo do século XX, outros estudiosos relataram vários aspectos da doença, embora a natureza da fisiopatologia ainda não tenha sido revelada2. Como a patogênese é pouco compreendida, diferentes origens para a doença foram postuladas. Infecção viral, disfunção imunológica e malignidade já foram sugeridas como mecanismos de desenvolvimento da doença. Algumas associações com distúrbios da tireoide também foram demonstradas4. Recentemente, a descoberta de frequentes mutações oncogênicas BRAF em LCH sustenta sua classificação como neoplasma10.
O pico de incidência de LCH ocorre entre 1 e 4 anos de idade; no entanto, pode se apresentar em todas as idades. Com uma incidência estimada de 4,0 a 5,4 casos por um milhão de crianças, seus dados epidemiológicos são difíceis de alcançar devido à raridade da doença11. Além disso, a LCH parece ser subdiagnosticada, pois pode ser assintomática ou confundida com outros distúrbios12.
A LCH afeta mais freqüentemente os tecidos ósseo, pulmonar, mucocutâneo, talâmico e linfático13. Na prática oftalmológica, o distúrbio envolve mais freqüentemente a órbita, representando menos de 1% das tumefações orbitais. A apresentação típica é de um inchaço palpebral superior em crescimento lento ao longo de um período de semanas a meses. A apresentação aguda é rara, geralmente surgindo devido a uma resposta inflamatória à lesão e pode ser confundida com celulite periorbitária ou dacrioadenite. Proptose, paralisia de nervo, papiledema e síndrome do seio cavernoso podem estar presentes na doença orbital14. A ocorrência de LCH na glândula lacrimal de paciente adulto foi relatada15. A pálpebra raramente é afetada.
O exame histológico revela células com citoplasma eosinofílico abundante e fundo de osinófilos, linfócitos, histiócitos e neutrófilos presentes em quantidades variáveis. O imunofenótipo de LCH inclui expressão do CD1a, proteína S100 e proteína langerina (CD207). O diagnóstico diferencial inclui sarcoma de células de Langerhans, outras lesões histiocíticas e linfoma. As características imunoistoquímicas e morfológicas descritas são geralmente suficientes para o diagnóstico16.
O tratamento de doença multissistêmica é baseado em protocolos e depende de algumas variáveis. A excisão completa da lesão pode ser curativa para doença cutânea focal. Esteróides e mostarda nitrogenada de psoraleno combinados com ultravioleta A (PUVA) são opções de tratamento de segunda linha. A radioterapia é uma opção quando as lesões são recorrentes ou progressivas 4. As lesões podem progredir para um processo crônico ou recidivante com remissão espontânea ou tratamento. A LCH limitada à pele tem excelente prognóstico geral17.
Como este relato de caso demonstra, a LCH pode estar limitada à pele e encontrada em locais únicos, como a pálpebra. Assim, deve ser considerada como um diagnóstico diferencial para lesões tumorais da pálpebra.
REFERÊNCIAS
1. Kumar V, Abbas AK, Fausto N, Mitchell R. Robbins & Cotran: Patologia. Rio de Janeiro: Elsevier; 2008.
2. Néel A, Artifoni M, Donadieu J, Hamidou M, Tazi A. Histiocytose langerhansienne de l’adulte. La Revue de Médecine Interne. 2015; 36:658-67.
3. Ramzan M, Yadav SP, Bhalla S, Jamwal P, Grover AK, Sachdeva A. Eyelid nodule: a rare presentation of langerhans cell histiocytosis. J Pediatr Hematol Oncol. 2012; 34:c158-c160.
4. Leveson J, Bourque JM, Lukovic J, Rashid Dar A. Radiotherapy for langerhans cell histiocytosis of bilateral eyelids. Cureus. 2016 Feb; 8(2):e474.
5. Takaura N, Inada N, Shoji J, Sawa M. Distribution of S-100 protein positive cells in conjunctiva. Nippon Ganla Gakkai Zasshi. 1995; 99:873-7.
6. Chikama T, Yoshino H, Nishida T, et al. Langerhans cell histiocytosis localized to the eyelid. Arch Ophthalmol. 1998; 116:1375-7.
7. Weissgold DJ, Wulc AE, Young M, et al. Eosinophilic granuloma of the eyelid. Ophthal Plast Reconstr Surg. 1994; 10:160-2.
8. Tosaka Y. A case of localized histiocytosis X of the eyelid. Nippon Ganka Gakki Zasshi. 1989; 93:103-8.
9. Daras C, Grayson W, Mayet I, et al. Langerhans’ cell histiocytosis of the eyelid. Br J Ophthalmol. 1995; 79:91-2.
10. Badalian-Very G, Vergilio JA, Fleming M, Rollins BJ. Pathogenesis of Langerhans cell histiocytosis. Annu Rev Pathol. 2013 Jan; 8:1-20.
11. Nicholson HS, Egeler RM, Nesbit ME. The Epidemiology of Langerhans cell histiocytosis. Hematol Oncol Clon Noth Am. 1988 Apr; 12(2):379-84.
12. Egeler RM, D’Angio GJ. Langerhans cell histiocytosis. J Pediatr. 1995 Jul; 127(1):1-11.
13. Howarth DM, Girlchrist GS, Mullan BP, et al. Langerhans cell Histiocytosis. Cancer. 1999; 85:2278-90.
14. Levy J, Monos T, Kapelushnik J, Maor E, et al. Ophthalmic manifestations in Langerhans cell histiocytosis. IMAJ. 2004; 6:553-5.
15. Pace ST, Gelman BB, Wong BR. Primary Langerhans cell histiocytosis of the lacrimal gland in an adult. Can J Ophthalmol. 2015 Jun; 50(3):e40-3.
16. Harmon CM, Brown N. Langerhans cell histiocytosis: a clinicopathologic review and molecular pathogenetic update. Arch Pathol Lab Med. 2015 Oct; 139(10):1211-4.
17. Ehrhardt MJ, Humphrey SR, Kelly ME, Chiu YE, Galbraith SS. The natural history of skin-limited langerhans cell histiocytosis: a single-institution experience. J Pediatr Hematol Oncol. 2014; 36:613-6.


Fonte de financiamento: declaram não haver
Parecer CEP: não aplicável
Conflito de interesses: declaram não haver
Recebido em:
19 de Junho de 2018.
Aceito em:
30 de Agosto de 2018.